La disfagia, una condizione caratterizzata da difficoltà nella deglutizione, richiede un'attenta gestione nutrizionale per garantire la sicurezza del paziente, prevenire la malnutrizione e migliorare la qualità della vita. Questa guida, basata su un'ampia raccolta di informazioni da fonti scientifiche e cliniche autorevoli (come dettagliato nella bibliografia), presenta gli approcci clinici e dietetici fondamentali per la nutrizione personalizzata nei pazienti con disfagia.
Indice dell'articolo
Classificazioni ed eziologia della disfagia
Sintomatologia e screening
1 INTRODUZIONE
La disfagia, definita come la difficoltà o l'incapacità di deglutire, rappresenta una condizione clinica complessa e multifattoriale che può influenzare significativamente la qualità di vita dei pazienti affetti. La deglutizione è un processo fisiologico fondamentale che coinvolge la coordinazione di muscoli e nervi per il trasferimento sicuro del cibo e dei liquidi dalla bocca allo stomaco. Un'interruzione di questo processo può portare a complicazioni gravi come malnutrizione, disidratazione e rischio di aspirazione polmonare.
Lo scopo di questa tesi è di esplorare la disfagia da diverse prospettive, iniziando con la descrizione dettagliata della patologia dal punto di vista anatomico e fisiologico. Successivamente, saranno esaminate le cause eziologiche della disfagia, che possono variare da condizioni neurologiche, malattie degenerative, a traumi ed interventi chirurgici, enfatizzando l’importanza di un approccio multidisciplinare nella gestione del trattamento di tale condizione.
Le aree di interesse comprendono l’analisi dei disturbi del gusto nei pazienti disfagici, descrivendone le cause, gli effetti e le strategie di gestione per mitigare questi sintomi, discutendo i protocolli di sintomatologia e screening, inclusi i metodi diagnostici per identificare precocemente la disfagia e monitorare il progresso del trattamento.
Inoltre, saranno analizzate le correlazioni tra disfagia e patologie tumorali, esaminando l'impatto dei tumori sulla funzione deglutitoria e le opzioni terapeutiche disponibili. Verrà affrontato il ruolo della nutrizione enterale come strategia di supporto nel paziente disfagico, delineando le modalità di somministrazione e i benefici terapeutici.
Si auspica che l’analisi approfondita delle strategie nutrizionali e terapeutiche, possa contribuire a migliorare la qualità di vita dei pazienti affetti da disfagia.
1.1 Cosa è la disfagia
Il termine "disfagia", che trae origine dalle parole greche dis (difficoltà) e fagia (mangiare), descrive una problematica nell'atto di alimentarsi. Più specificamente, si riferisce alla difficoltà nel deglutire cibi solidi, liquidi o semisolidi, i quali faticano a transitare correttamente dal cavo orale allo stomaco. Tale condizione clinica, pur non essendo una patologia a sé stante ma piuttosto un sintomo di svariate affezioni, mostra una crescente incidenza. Essa comporta significative ripercussioni a livello sociale, sanitario ed economico, e frequentemente risulta sottostimata e gestita in modo inadeguato nei diversi contesti assistenziali. Attualmente, si osserva una marcata eterogeneità negli approcci diagnostici, terapeutici e assistenziali, attribuibile in gran parte a una formazione non ottimale degli operatori sanitari. La disfagia si configura come un disturbo diffuso, potendo insorgere a qualsiasi età, sebbene la sua prevalenza sia più elevata nella popolazione anziana.
Le cause possono risiedere in alterazioni funzionali o strutturali del cavo orale, della faringe, dell'esofago o dello sfintere esofageo inferiore (cardias). Di conseguenza, la disfagia può essere categorizzata secondo criteri anatomici o fisiopatologici: la classificazione anatomica si basa sulla localizzazione dell'origine del disturbo, mentre quella fisiopatologica considera i meccanismi che compromettono la deglutizione. Si configura come un quadro clinico complesso, il cui manifestarsi, decorso e severità sono influenzati dalla patologia sottostante (sia essa un disturbo medico, l'esito di un intervento chirurgico o il fisiologico processo di invecchiamento – definito presbifagia) e dalla coesistenza di altre patologie. Frequentemente, è correlata a una disfunzione del sistema digerente che comporta un anomalo passaggio del bolo alimentare attraverso le prime vie digestive. Dal punto di vista assistenziale, la disfagia assume una rilevanza notevole, poiché può compromettere, talvolta fino a impedire, un'alimentazione orale autonoma e sicura.
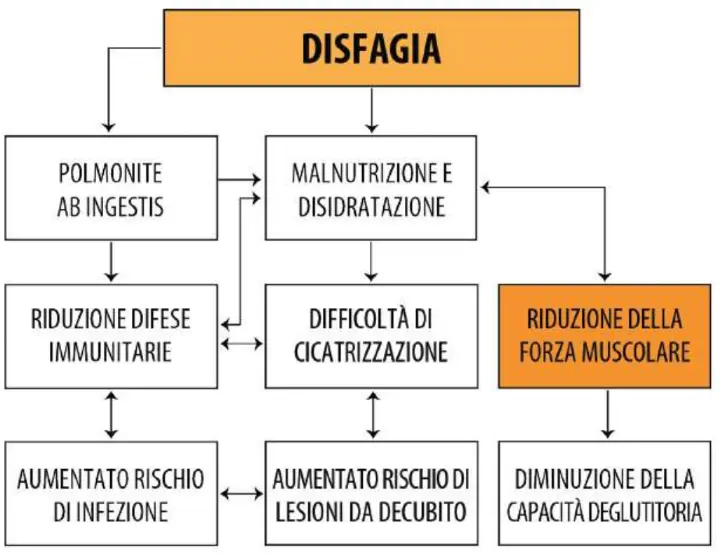
Le eziologie della disfagia si distinguono principalmente in neuromuscolari e strutturali. Condizioni neuromuscolari frequentemente associate alla disfagia includono miastenia gravis, sclerosi multipla, distrofie muscolari, malattia di Huntington, ictus cerebrale, morbo di Parkinson e malattia di Alzheimer. Le neoplasie del distretto testa-collo rappresentano, invece, le cause strutturali predominanti. Nelle forme severe, il soggetto disfagico può incontrare difficoltà nell'assumere un apporto alimentare qualitativamente e quantitativamente adeguato, esponendosi a rischi quali malnutrizione, disidratazione e aspirazione di cibo nelle vie aeree, con potenziali complicanze severe, tra cui le polmoniti ab ingestis.
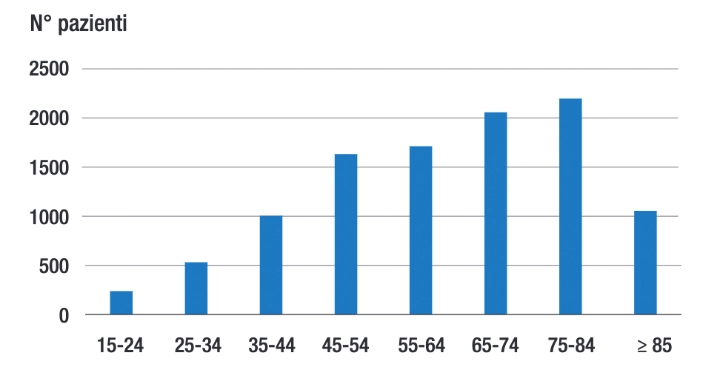
A livello epidemiologico, la disfagia interessa circa il 13% della popolazione generale dopo i 65 anni d’età e che 1 persona su 17 ne soffra prima o poi nel corso della vita. La percentuale sale al 50% o più nei soggetti anziani ospedalizzati o in RSA e si manifesta nel 40-70% delle persone che hanno subito un ictus (1). Nei pazienti con ictus e malattie neurologiche cronico-degenerative, come l’Alzheimer, il Parkinson, la demenza e la SLA, può comparire in percentuali comprese tra 20-80% dei casi.
Con l'avanzare dell'età, possono insorgere alterazioni della sensibilità oro-faringo-laringea, cambiamenti nella dentizione, debolezza (ipostenia) e incoordinazione muscolare, nonché disregolazioni a carico del sistema nervoso. Nell'individuo anziano si osserva un prolungamento significativo della durata totale dell'atto deglutitorio. Si riscontrano altresì una diminuzione della produzione salivare e della forza muscolare, unitamente a una riduzione della frequenza degli atti deglutitori in un dato intervallo temporale. Questo quadro complessivo, legato all'invecchiamento fisiologico della deglutizione, è noto come presbifagia.
Benché la disfagia interessi prevalentemente la popolazione anziana, può manifestarsi anche in soggetti più giovani, talvolta accompagnata da dolore (odinofagia) e come esito di disturbi primari di natura ostruttiva o motoria, quali neoplasie o acalasia. Questa condizione compromette gli organi e le strutture deputate alla deglutizione, quel meccanismo che permette il passaggio di alimenti e liquidi dalla bocca allo stomaco per la digestione.
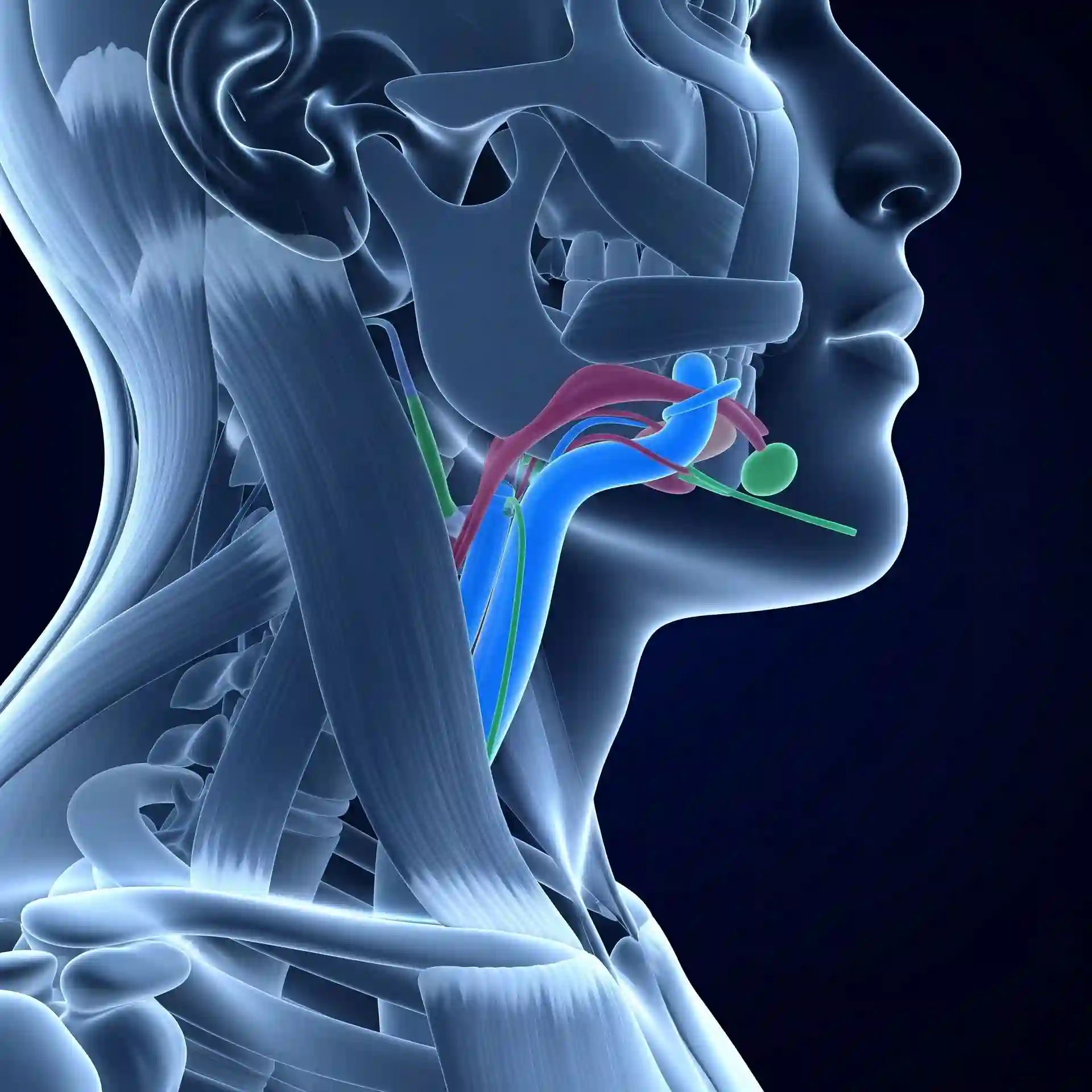
Per comprendere le alterazioni deglutitorie, è essenziale richiamare la fisiologia di questo complesso atto, governato da sei dei dodici nervi cranici che innervano il distretto cervico-facciale e parte delle spalle. Il processo deglutitorio è un'attività neuromuscolare estremamente complessa, orchestrata da diversi nervi cranici (trigemino, facciale, glossofaringeo, vago, ipoglosso) e coinvolge circa 55 muscoli, radici cervicali e specifiche aree cerebrali motorie e sensitive. Tra i muscoli cruciali vi sono quelli masticatori, come massetere, temporale e pterigoidei (innervati dal trigemino), e quelli che abbassano la mandibola, quali miloioideo, genioioideo e digastrico (quest'ultimo con innervazione mista dal nervo miloioideo e faciale).
La deglutizione è intrinsecamente legata alle funzioni respiratoria e fonatoria, non essendo unicamente un meccanismo di propulsione alimentare. Vie aeree e digestive condividono un tratto comune, l'oro- e l'ipofaringe, formando il cosiddetto quadrivio faringeo. Qui, il bolo alimentare, adeguatamente preparato, deve essere correttamente indirizzato verso l'esofago, proseguendo poi fino allo stomaco. Normalmente, l'atto deglutitorio si ripete circa 600 volte al giorno, si completa in circa 15 secondi e gestisce in modo coordinato il transito di sostanze di varia consistenza. Si articola convenzionalmente in quattro fasi: preparatoria, orale, faringea ed esofagea. La fase preparatoria inizia con stimoli sensoriali (olfattivi, visivi, legati alla presentazione dell'alimento) che inducono modificazioni secretorie salivari e del tono muscolare orale.
Successivamente, con l'introduzione del cibo nel cavo orale, inizia la fase orale volontaria: muscoli masticatori e lingua processano l'alimento con la saliva per formare un bolo adeguato. La lingua poi lo spinge posteriormente verso l'ipofaringe (o laringofaringe), mentre il palato molle si solleva per impedire il reflusso nasale nel rinofaringe. L'arrivo del bolo nell'orofaringe stimola recettori che innescano la fase faringea, involontaria e riflessa. Questa comporta una sequenza coordinata: elevazione antero-superiore della laringe, abbassamento dell'epiglottide a protezione delle vie aeree, contrazione dei muscoli faringei per spingere il bolo oltre lo sfintere esofageo superiore (che si rilascia tempestivamente) e progressione tramite peristalsi nell'esofago prossimale, fino al superamento dello sfintere esofageo inferiore.
Questa complessa serie di eventi, finemente regolata a livello nervoso, richiede precisione temporale e sequenziale; l'inefficienza di un singolo componente, anatomico o funzionale, può compromettere l'intero meccanismo. Le fasi deglutitorie di maggiore criticità e interesse clinico sono quelle centrali, dalla preparazione intraorale del bolo (influenzata da consistenza, temperatura e viscosità) alla fase riflessa faringea, che assicura il transito del bolo mediante la propulsione linguale e la contrazione faringea, sotto il controllo dei centri nervosi dedicati.
Le principali alterazioni ed i problemi di carattere anatomo-fisiologico nel meccanismo di deglutizione indotti dalla disfagia riguardano tutto il coordinamento di diversi muscoli e strutture coinvolte. Principalmente parliamo di bocca, faringe, laringe ed esofago. La bocca è sede del palato molle, della lingua, dei denti e dei muscoli. Masticatori. La faringe include l'orofaringe e l'ipofaringe, con muscoli faringei che aiutano a spingere il bolo verso l'esofago. La laringe con l’epiglottide si chiude per prevenire l’aspirazione del cibo nelle vie respiratorie. Ed infine l’esofago, un tubo muscolare che trasporta il cibo dallo sfintere esofageo superiore allo stomaco. Le alterazioni anatomo-fisiologiche indotte dalla disfagia coinvolgono in prima battuta sia la lingua che la bocca, infatti è possibile evidenziare debolezza dei muscoli della lingua e dei muscoli masticatori, compromettendo la formazione del bolo la sua propulsione verso la faringe. Questo può risultare in un'inefficace masticazione e preparazione del cibo per la deglutizione. Nella faringe le alterazioni possono includere una ridotta coordinazione muscolare e una forza insufficiente nei muscoli faringei, compromettendo il passaggio del bolo dall'orofaringe all'esofago. Questo può causare ritardi nella deglutizione e rischi di aspirazione. La disfagia compromette anche le funzioni della laringe, interferendo con la chiusura dell'epiglottide, aumentando il rischio di aspirazione del cibo nelle vie respiratorie. I muscoli laringei potrebbero non funzionare correttamente, riducendo la protezione delle vie aeree durante la deglutizione. Nell’esofago le alterazioni possono includere disturbi della motilità, come l'acalasia, dove la peristalsi esofagea è compromessa e lo sfintere esofageo superiore non si apre correttamente. Questo può causare difficoltà nel transito del bolo verso lo stomaco e sensazioni di ostruzione.
Nel dettaglio anatomo-fisiologico le interferenze riguardano i muscoli masticatori, lo sfintere esofageo superiore la cui funzione consente il passaggio del cibo dall’esofago allo stomaco e l’epiglottide. Per ciò che riguarda i muscoli masticatori, la disfagia causa debolezza, paralisi, e questo può impedire la formazione efficace del bolo. Parlando invece dell’epiglottide sappiamo che il suo malfunzionamento può causare, come vedremo più avanti nel dettaglio, problemi di aspirazione di cibo durante la deglutizione causando gravi problemi alle vie respiratorie. Le strutture anatomo-fisiologiche coinvolte nel processo della deglutizione quindi, ricoprendo un ruolo complesso caratterizzato da una cronologia di azioni rapidissime fanno riferimento andando ancor più nel dettaglio ai muscoli della masticazione, della lingua, dei muscoli faringei, dello sfintere esofageo superiore e dell’epiglottide. Parlando dei muscoli della masticazione facciamo riferimento al Masseter, responsabile della chiusura della mandibola e della masticazione. La disfagia può causare debolezza o paralisi del masseter . Parliamo del Temporale, muscolo aiuta nella depressione della mandibola e nella masticazione. La disfagia può ridurre la forza e la coordinazione del temporale. Per ciò che concerne i muscoli della lingua evidenziamo il Genioglosso, cruciale per la mobilità della lingua e la formazione del bolo alimentare. La disfagia può causare debolezza o paralisi del genioglosso, rendendo difficile la manipolazione del cibo nella bocca. Infine lo Stiloglosso: questo muscolo aiuta a sollevare la parte posteriore della lingua durante la deglutizione. La disfagia può compromettere la funzione del stiloglosso, influenzando il passaggio del bolo dalla bocca alla faringe. I muscoli faringei sono il Constrictores faringei ed il Palatofaringeo. Il primo è responsabile della propulsione del bolo verso l'esofago. La disfagia può causare debolezza o disfunzione dei constrictores faringei, portando a difficoltà nella deglutizione. Mentre il Palatofaringeo aiuta a chiudere la nasofaringe durante la deglutizione. Nella disfagia può ridursi la forza e la coordinazione di questa struttura anatomica con aumento del rischio di aspirazione nasale. Lo Sfintere esofageo superiore si apre per consentire il passaggio del bolo dall'esofago allo stomaco, in questo caso assistiamo a disfunzione dell'UES, portando a difficoltà nel transito del cibo e sensazioni di ostruzione.
L’Epiglottide protegge le vie respiratorie durante la deglutizione, chiudendosi sopra l'entrata laringea. La disfunzione dell’epiglottide ,causata dalla disfagia, aumenta il rischio di aspirazione del cibo nelle vie respiratorie.
Risulta chiaro come la panoramica di anomalie fin’ora descritte possa concatenarsi a tutta una serie di eventi che dal punto di vista funzionale caratterizzano l’atto motorio della deglutizione e che nella disfagia vedono debolezza muscolare, incoordinazione motoria, disturbi della motilità esofagea, ed infine ostruzioni meccaniche.
La disfagia può causare danni anche gravi alla salute, quindi è fondamentale riconoscerla il più precocemente possibile. Capire se la difficoltà a deglutire cibo e/o bevande sia accidentale o sintomatica di vera e propria disfagia non è sempre semplice ed è comunque compito di uno specialista. La presenza frequente di uno o più dei seguenti segnali indicati in questa scheda, durante o subito dopo i pasti, indica comunque quando è il caso di rivolgersi al medico. Di seguito, una semplice scheda da consegnare al paziente con un elenco dei principali segnali che, se si presentano spesso durante o subito dopo i pasti, indicano ai familiari e/o ai caregiver, quando è il caso di rivolgersi al medico.
Data la potenziale gravità delle conseguenze della disfagia sulla salute, il suo riconoscimento tempestivo è cruciale. Distinguere una difficoltà deglutitoria occasionale da una vera e propria disfagia sintomatica può essere complesso e richiede una valutazione specialistica. Tuttavia, la manifestazione ricorrente di specifici segnali d'allarme, osservabili durante o immediatamente dopo l'assunzione di cibo e/o liquidi, dovrebbe indurre a consultare un medico. Per facilitare l'identificazione di tali campanelli d'allarme da parte di pazienti, familiari o caregiver, è utile fornire un elenco sintetico dei principali indicatori che suggeriscono la necessità di un approfondimento medico.
2 Classificazioni ed eziologia della disfagia
La disfagia può essere classificata come organica, se originata da lesioni strutturali lungo il tragitto del bolo dal cavo orale allo stomaco, o funzionale, se derivante da un’alterata motilità muscolare del tratto digestivo superiore. Può presentarsi occasionalmente, ad esempio per una masticazione inadeguata, oppure essere conseguenza di patologie con eziologia metabolica, infettiva, neurologica, miopatica, strutturale o iatrogena. Le cause specifiche possono variare anche in base alla localizzazione del difetto nel processo deglutitorio.
Sebbene un approccio comune sia classificare la disfagia in base alla sede anatomica del malfunzionamento, è importante considerare anche altri fattori e criteri.
Criteri di classificazione della disfagia
Criterio eziologico
Considera l'origine della patologia, distinguendo forme malformative, infettive, degenerative, vascolari, dismetaboliche, neoplastiche, tossiche, traumatiche e iatrogene. Esempi specifici includono la disfagia da anello di contrazione, la disfagia lusoria (dovuta a compressione esofagea da anomalie vascolari toraciche) e la disfagia maligna (causata da stenosi esofagea per crescita tumorale). Esistono anche la disfagia psicogena, in assenza di ostacoli fisici, e la disfagia sideropenica (Sindrome di Plummer-Vinson).
Criterio patogenetico
Classifica la disfagia in base al meccanismo alterato, identificando disfagie meccaniche, motorie, respiratorie e psichiatriche.
Criterio Fisiopatologico (basato sulla fase deglutitoria compromessa)
Disfagia Faringea: Interessa la terza fase della deglutizione ed è frequentemente (80% dei casi) associata a malattie neurologiche, mentre il restante 20% è spesso esito di interventi chirurgici. Questa forma comporta rischi elevati di aspirazione tracheobronchiale. I sintomi tipici includono: fuoriuscita di cibo/liquidi dal naso, tosse, starnuti, alterazioni vocali post-deglutitorie, frequenti schiarimenti di gola, segni di soffocamento, dispnea durante i pasti, affaticamento e deglutizione ritardata o dolorosa. Il riconoscimento precoce è fondamentale per un trattamento tempestivo e la riduzione delle complicanze.
Disfagia Esofagea: Si verifica quando è compromessa la quarta fase deglutitoria. Cause comuni sono diverticoli esofagei, compressione da gozzo tiroideo, patologie neurologiche, esiti chirurgici, e il processo di invecchiamento (con riduzione della forza muscolare propulsiva). Altre eziologie includono stenosi esofagea, reflusso gastroesofageo, disturbi della motilità esofagea, gastrite, ulcera peptica e tumori gastrici.
Nei neonati e bambini, la disfagia può essere legata a prematurità, basso peso alla nascita, malformazioni congenite (es. labioschisi, palatoschisi) o disturbi neurologici. In alcuni casi, l'eziologia rimane non identificata.
Disfagia Orale: Si manifesta per alterazioni della prima o seconda fase deglutitoria. Può derivare, ad esempio, da paralisi del nervo facciale, labiopalatoschisi, o frequentemente da esiti di chirurgia demolitiva o radioterapia del distretto orale.
Criterio topografico
Distingue le forme di disfagia in base alla localizzazione della lesione nervosa o muscolare: orofaringea, esofagea, da lesione del primo o secondo motoneurone, da compromissione dell'innervazione sensoriale, o da lesione dell'effettore muscolare/neuromuscolare.
Altre cause e fattori contribuenti
La disfagia può anche insorgere come effetto collaterale di farmaci, la cui assunzione può influenzarne la severità, o come conseguenza di interventi chirurgici e trattamenti radioterapici. Ad esempio, l'uso di oppiacei, specialmente in pazienti con disturbi psichiatrici o Parkinson, può indurre alterazioni motorie esofagee (ipercontrattilità/ipertensione) simili all'acalasia di tipo III.
Complicazioni possono derivare da:
Chirurgia del cavo orale: con possibile perdita del controllo linguale e difficoltà masticatorie/deglutitorie.
Chirurgia faringo-laringea: con difficoltà nel transito di liquidi e solidi.
Radioterapia: che può causare dolore, xerostomia (ridotta salivazione), secchezza delle mucose e limitazione dei movimenti.
Identificare i fattori di rischio e i segni della disfagia, osservare il paziente durante i pasti, valutare la dieta e lo stato nutrizionale/idratazione sono passaggi cruciali. Cause ostruttive, rilevabili tramite fibroscopia, e fattori reumatologici possono altresì contribuire. Numerose classi farmacologiche sono implicate nell'insorgenza della disfagia, tra cui: atropina, antipsicotici (es. clorpromazina), SSRI (fluoxetina, sertralina), triciclici (amitriptilina), aminoglicosidi, steroidi, antiepilettici, benzodiazepine, miorilassanti, analgesici oppioidi (es. codeina), bifosfonati e FANS (ibuprofene, ketoprofene). Questi farmaci possono agire attraverso depressione del SNC, xerostomia, miopatia, riduzione del controllo muscolare volontario, alterazione della motilità esofagea, o causando ulcerazioni/irritazioni mucosali.
L'entità del disturbo disfagico può dipendere anche da interazioni farmacologiche, che possono amplificare effetti avversi, agire come effetti collaterali diretti, alterare l'azione terapeutica o causare tossicità diretta alle strutture deglutitorie.

3 Sintomatologia e screening
3.1 Sintomatologia
Per ciò che riguarda i campanelli d’allarme avremo sicuramente fastidio o dolore durante la deglutizione, allungamento del tempo associato al pasto, senso di corpo estraneo in gola, tosse durante il pasto, alterazione della voce dopo la deglutizione, progressivo cambiamento delle abitudini alimentari che avrà rilevanza nella consistenza del cibo e nelle quantità.
Anche il calo ponderale senza cause apparenti può rappresentare un campanello di allarme, specialmente se associato ad uno o più fattori tra quelli sopra elencati. Dunque alla luce di questo scenario risulta comprensibile l’assoluta consapevolezza del problema al fine di evitare l’insorgenza di altri problemi non indifferenti, proprio perchè i segni della malattia non è detto risultino evidenti in tutte le circostanze. Spesso il sintomo può essere appena percettibile e questo determina un ritardo nei tempi di attivazione per le terapie adeguate. Soprattutto in caso di deglutizione dolorosa e globus, condizioni indipendenti ma a volte compresenti, si rende necessaria la cosiddetta diagnosi differenziale. L’odinofagia (deglutizione dolorosa) rappresenta un sintomo abbastanza distintivo di carcinoma sebbene abbia anche numerose altre cause non correlate al cancro. Esiste ancora una ulteriore cascata sintomatologica che all’esame obiettivo del medico sarà utile alla diagnosi della disfagia. Ecco in questo caso quali sono i segni tangibili: alterato livello di coscienza, linguaggio mal articolato, gestione difficoltosa delle secrezioni orali, ridotta funzione laringea, dispnea. Solitamente la prima figura a formulare il sospetto di una disfagia è il medico curante. La diagnosi viene fatta sulla base di alcuni importanti segni d’allarme che si evincono durante l’esame obiettivo. In alcuni casi sarà utile effettuare lo screening della capacità deglutitoria.
3.2 Screening
Lo screening solitamente può essere effettuato dal medico di base o dal personale infermieristico opportunamente formato. La visita deglutologica sarà condotta dal foniatra e dall’otorinolaringoiatra e dai medici che abbiano conseguito il master in Deglutologia. In ogni caso è utile dire che solo un team multidisciplinare sarà in grado di riconoscere adeguatamente il disturbo della disfagia, in questo modo sarà possibile avviare tutte le terapie necessarie che comprendono sia quelli nutrizionali che riabilitativi - terapeutici.
Sarà quindi opportuno in fase di screening, valutare come prima cosa la capacità deglutitoria del paziente attraverso quattro fasi principali: nello step 1 si dovrà comprendere se il paziente è in grado di controllare la saliva e di collaborare, oltre a ciò è da verificare se lo stesso è sveglio e vigile. Durante lo step numero 2 si valuterà se il paziente riesce a leccarsi le labbra, se riesce a respirare normalmente e se presenta una tosse volontaria.
Lo step numero 3 riguarderà l’igiene orale. L’ultimo step, il numero 4, è quello relativo al bolo d’acqua che può essere eseguito sia in ambulatorio che a domicilio. Questo test individua i soggetti che sono a rischio di inalazione.
Chiaramente il test risulta alterato se il paziente non è in grado di rispondere alle condizioni sopra descritte.
Test del bolo d’acqua: consiste nella somministrazione di un piccolo volume di acqua e nell’osservazione dell’inizio della deglutizione e dell’eventuale comparsa di tosse o di alterazione della qualità della voce. Il paziente sarà in posizione seduta o se allettato dovrà avere il busto elevato ad almeno 80 gradi. Si somministra un cucchiaino di acqua naturale a temperatura ambiente per almeno tre volte posizionando delicatamente il dito sulla laringe per avvertirne il sollevamento durante l’atto deglutitorio.
Se il paziente tiene troppo l’acqua in bocca prima di deglutire, se tossisce prima, durante o dopo la deglutizione oppure se la voce è cambiata durante la deglutizione, sarà da considerare un segno di alterazione del test.
Se il test risulta normale in questa fase, si osserva mentre beve senza interruzioni un bicchiere d’acqua un sorso alla volta. Se in una qualsiasi fase del test vi è assenza della deglutizione, comparsa di tosse, oppure tosse ritardata o ancora alterazioni della qualità della voce invitando il paziente a fare un vocalizzo con la A prolungata, il test è considerato alterato. In questa circostanza si richiede attuazione di provvedimenti cautelari e l’avvio del paziente a consulenza specialistica foniatrica e nutrizione clinica.
3.3 Valutazione strumentale
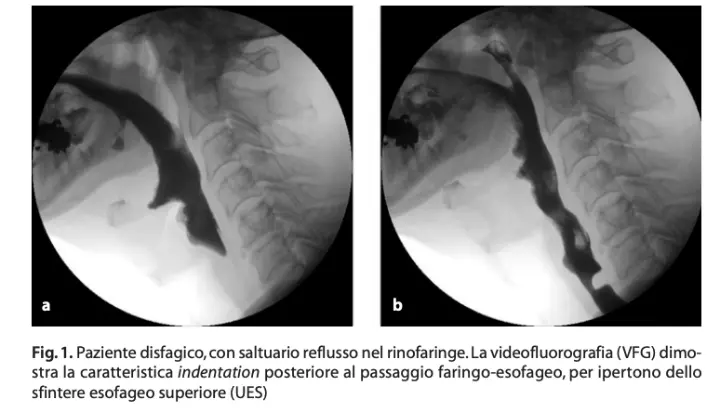
Per una diagnosi precisa e tempestiva della disfagia, la valutazione specialistica si avvale di tecnologie avanzate. Tra gli strumenti utilizzati figurano la videoregistrazione fluoroscopica, la scintigrafia oro-faringea, l'elettromiografia della deglutizione, la manometria, la pH-metria esofagea e l'ultrasonografia del collo. Tuttavia, le linee guida indicano la videofluorografia digitale (VFG) e lo studio fibroendoscopico della deglutizione (FEES) come gli esami più efficaci.
Le tecniche di acquisizione d'immagine sono evolute significativamente, passando da immagini singole a filmati radioscopici, fino alle recenti metodiche digitali. Queste ultime permettono di registrare l'intero processo deglutitorio, dall'introduzione orale del cibo al suo passaggio nello stomaco e nelle prime anse intestinali, con ricostruzioni dinamiche fino a 15 fotogrammi/secondo e oltre, a dosi di radiazioni ridotte per il paziente.
La Videofluorografia (VFG) è considerata il gold standard per la valutazione strumentale della deglutizione, sebbene la sua diffusione sia limitata dalla necessità di apparecchiature sofisticate e personale altamente qualificato. È un esame radiologico dinamico, non invasivo, ben tollerato, di breve durata (pochi minuti) ed eseguito nel rispetto delle norme di radioprotezione, esponendo il paziente a minime dosi radiogene. La VFG consente una valutazione accurata di tutte le fasi deglutitorie, monitorando anche la motilità esofagea, la presenza di patologie endoluminali, la posizione della giunzione gastroesofagea e l'eventuale ernia iatale. Questo esame è inoltre cruciale per identificare le strategie riabilitative più idonee a migliorare l'efficienza deglutitoria e ridurre il rischio di aspirazione, correlando eventi pressori e propagazione del bolo radiopaco. È indicato in pazienti con disfagia oro-faringea, disturbi delle prime fasi deglutitorie e problematiche dispeptiche, utilizzando boli di varia consistenza e dimensione.
Il paziente deve presentarsi a digiuno. Durante l'esame, viene invitato a deglutire una sospensione semiliquida di solfato di bario, un mezzo di contrasto che opacizza le superfici, rendendole visibili radiologicamente. La VFG è particolarmente utile nello studio del reflusso gastroesofageo e nel follow-up post-chirurgico dell'ernia iatale. La manovra di Trendelenburg può essere utilizzata nella fase finale per evidenziare reflussi.
L'esame è eseguibile con qualsiasi apparecchio telecomandato analogico (con videoregistrazione) o digitale (minimo 30 frame/secondo), rendendolo accessibile in molti reparti di Radiologia. È preferibile disporre di una pedana mobile per facilitare il posizionamento di pazienti instabili, in sedia a rotelle o barellati (mantenendo adeguata distanza tubo-detettore). Angolazioni del tubo possono compensare posture anomale del capo. Sebbene esistano protocolli standardizzati, la scelta del tipo e consistenza del contrasto, nonché la postura del capo, sono spesso personalizzate in base alla sintomatologia, autonomia alimentare e collaborazione del paziente, considerando sempre la postura di testa e collo. Uno screening iniziale può prevedere la somministrazione di almeno 5ml di alimenti a diversa consistenza, miscelati con bario.
Riguardo al mezzo di contrasto, mentre negli USA è disponibile il Varibar®, in Italia si utilizza comunemente il bario HD, miscelato con acqua (circa 60 ml) per ottenere una consistenza simile allo yogurt, ulteriormente diluibile o addizionabile a cibi solidi (pane, fette biscottate).
Tecnicamente, si utilizzano proiezioni latero-laterale (LL) e antero-posteriore (AP). La proiezione LL, sfruttando il contrasto aereo naturale di rino- e orofaringe, permette di studiare la morfologia di base linguale, epiglottide e palato molle; si valuta dinamicamente anche la motilità del velo palatino durante la fonazione (es. pronunciando "candy"). La proiezione AP senza contrasto è utile per lo studio della motilità cordale durante la fonazione (es. vocale "iiii").
Successivamente, si introduce il bario. Piccole quantità aspirate non hanno solitamente rilevanza clinica, venendo eliminate in poche ore. Tuttavia, in caso di rischio di aspirazione massiva o in pazienti con ridotto stato di coscienza, è preferibile un mezzo di contrasto non ionico per evitare complicanze. È controindicato l'uso di mezzi di contrasto iodati-ionici iperosmolari, per il rischio di edema polmonare in caso di aspirazione. Si inizia con piccole quantità di contrasto, aumentandole progressivamente per minimizzare il rischio di aspirazione. La somministrazione di boli a diverse consistenze è fondamentale per identificare le cause di disfagia selettiva, le consistenze responsabili di aspirazione, differenziare l'aspirazione mono-consistenza da quella multi-consistenza (più grave) e individuare le consistenze più sicure per una successiva rieducazione alimentare orale. In pazienti con marcata cifosi dorsale, una proiezione obliqua può facilitare la visualizzazione dell'apertura dello sfintere esofageo superiore e dell'esofago cervicale. Variazioni della postura del capo possono rivelare anomalie non evidenti in posizione neutra e aiutare a identificare manovre compensatorie. È consigliabile estendere la valutazione del transito fino alla giunzione esofago-gastrica, specialmente negli anziani.
L'esame va sospeso in caso di ostruzione completa delle vie aeree/digestive, laringo/broncospasmo, aspirazione di contenuto gastrico, o assenza di meccanismi protettivi delle vie aeree.

Lo studio endoscopico della deglutizione (FEES) impiega un nasofaringoscopio introdotto attraverso una fossa nasale fino al faringe. Permette lo studio diretto della sola fase faringea (eccetto il momento del "whiteout"), fornendo informazioni indirette sulle fasi orale ed esofagea. La FEES è elettiva per lo studio dello sfintere laringeo e della sensibilità, oltre alla visualizzazione e gestione dei ristagni. È meno invasiva della VFG, eseguibile al letto del paziente anche in condizioni instabili, e dovrebbe essere condotta da foniatri o personale esperto in fisiopatologia e riabilitazione deglutitoria. Valuta la fase 3, lo stato locale post-deglutitorio, e rileva penetrazione, aspirazione e ristagni.
Altre metodiche dinamiche includono la manofluorografia (radiologia + misurazione pressoria faringea) e la scintigrafia (progressione di un bolo marcato radioattivamente). L'auscultazione cervicale, che consiste nell'ascoltare con uno stetoscopio i rumori respiratori e deglutitori a livello laringeo, non ha attualmente solide evidenze scientifiche a supporto del suo utilizzo per lo studio della disfagia, necessitando di ulteriore ricerca.

4 Disfagia in Oncologia
La disfagia nel paziente oncologico costituisce una sfida centrale per la medicina riabilitativa, trattandosi di una condizione più diffusa di quanto comunemente percepito e caratterizzata da quadri clinici variabili per gravità ed espressione. Tali manifestazioni sono determinate dall'interazione di molteplici fattori concorrenti, i quali, in relazione allo stadio patologico e al contesto specifico, possono agire come elementi predisponenti, aggravanti o assumere rilevanza prognostica. Il modello di valutazione della disabilità impiegato in ambito oncologico si dimostra pertinente anche per l'analisi del disturbo deglutitorio.
Nello schema di valutazione della disabilità nel paziente oncologico, la disabilità scaturisce dall'interazione di diversi elementi, e l'analisi di ciascun fattore è cruciale per pianificare un percorso riabilitativo integrato. Tale modello guida il riabilitatore a considerare tutte le variabili pertinenti, adattate al contesto oncologico. L'assessment del paziente si basa quindi su quattro aspetti chiave: le caratteristiche della neoplasia (come sede, dimensioni e biologia), i trattamenti oncologici effettuati (chirurgia, chemio/radioterapia, terapie biologiche), le condizioni cliniche e le comorbidità preesistenti, e infine gli aspetti psico-sociali, ovvero le attitudini del paziente verso la malattia e le risorse da lui impiegate.
La disponibilità o meno di un caregiver dedicato, in grado di fornire il sostegno richiesto, rappresenta un supporto esterno ma intimamente connesso al paziente, e deve essere attentamente valutata. Nel contesto oncologico, il rapporto temporale tra le cause e l'insorgenza della disfagia presenta caratteristiche distintive.
Subito dopo la diagnosi, o nelle fasi iniziali, la consapevolezza consolidata degli effetti dei trattamenti antitumorali (chirurgici, farmacologici e radioterapici) impone un monitoraggio proattivo del paziente. Tale approccio mira ad anticipare le problematiche, adottando progressivamente misure preventive, di contenimento o terapeutiche per la disabilità che ne potrebbe derivare. Diversamente, nel corso del follow-up, anche a distanza di anni dal termine delle terapie, l'apparizione di un disturbo deglutitorio potrebbe non essere immediatamente ricondotta alla pregressa patologia neoplastica. In tali circostanze, si rende talvolta indispensabile un atteggiamento analitico e investigativo per stabilire il nesso causale. È quindi necessario approfondire la situazione, considerando anche segni non direttamente collegati alla deglutizione, come dolore, calo ponderale o disturbi digestivi, specialmente in pazienti con anamnesi di neoplasie localizzate in altre sedi o diffuse, quali linfomi o mieloma multiplo. Spesso si tratta di manifestazioni sintomatologiche di lieve entità e ben tollerate che, tuttavia, in assenza di una valutazione clinico-funzionale e di un intervento riabilitativo, possono determinare un progressivo deterioramento della qualità di vita.
Il tumore può essere responsabile dello sviluppo di disfagia in diversi modi: direttamente, quando si propaga nelle aree coinvolte nei processi fisiologici della deglutizione, come nel caso delle neoplasie che coinvolgono testa collo, esofago e cardias. In questi casi possiamo assistere ad occlusioni meccaniche ad esordio graduale ed ingravescente.
Anche tumori apparentemente distanti dal punto di vista della regione anatomica possono produrre l’insorgenza di questa disfunzione attraverso una compressione estrinseca. Alcuni esempi possono essere i tumori polmonari, mediastinici, retrofaringei e tiroidei. In ogni caso la disfagia è un sintomo comune in diverse forme di cancro, soprattutto quelli che coinvolgono l'esofago e le strutture adiacenti. Una descrizione dettagliata delle forme di cancro in cui si presenta più frequentemente la disfagia, descrive il tumore all’esofago come una delle forme principali, causa di disfagia. Esistono due tipi principali di cancro esofageo: Carcinoma a Cellule Squamose che si sviluppa nella parte superiore dell’esofago e rappresenta la forma più comune di cancro esofageo. La disfagia si manifesta quando il tumore cresce e comprime l'esofago, rendendo difficile il passaggio del cibo.
Mentre l’Adenocarcinoma è un tipo di cancro che si sviluppa nella parte inferiore dell'esofago, spesso associato alla malattia da reflusso gastroesofageo. La disfagia si verifica quando il tumore ostruisce il lume dell’esofago. Inoltre alcuni tipi di cancro della testa e del collo possono causare disfagia, tra cui il Carcinoma della Laringe, che può comprimere l'esofago, causando difficoltà a deglutire ed il Carcinoma della Ghiandola parotide che può crescere e comprimere l'esofago, portando alla disfagia.
Alcuni tumori toracici possono causare disfagia, soprattutto quelli che si trovano vicino all’esofago. Parliamo del Carcinoma Polmonare, un tumore al polmone può crescere e comprimere l'esofago, causando difficoltà a deglutire, e dei Tumori Mediastinici, che si sviluppano nel mediastino possono comprimere l'esofago, portando altresì alla disfagia.
Anche alcuni cancri della pelle, se sviluppati nelle aree adiacenti all’esofago possono aumentare il rischio di disfagia, come ad esempio il Melanoma.
Il Carcinoma della testa del pancreas è un tipo di cancro che può crescere e comprimere l'esofago, portando alla disfagia.
Infine anche se meno comune, il cancro del colon può causare disfagia se si metastatizza alle strutture adiacenti all’esofago. Queste sono alcune delle principali forme di cancro in cui si presenta frequentemente la disfagia, ogni tipo di cancro può avere diverse cause e meccanismi che portano al disturbo, ma il comune denominatore è la compressione o l'ostruzione dell'esofago da parte del tumore.
Lesioni localizzate del sistema nervoso possono altresì produrre disfunzione riguardante il processo della deglutizione. Ad esempio, la lesione dei nervi cranici V, VII, VX, X, XII. In relazione e sulla base del distretto nervoso interessato o compromesso dalla lesione, avremo una disfagia alta o bassa, che avrà quadri diagnostici e clinico funzionali differenti.
In questo panorama, la disfagia alta rappresenta la disfunzione più suscettibile rispetto alle possibili terapie riabilitative.
All’interno della tabella è possibile valutare i parametri delle relative disfunzioni.
Al contrario la disfagia bassa non risulta facilmente aggredibile con gli strumenti della medicina riabilitativa.
Dunque al fine di tracciare una panoramica generale legata a questo frangente, possiamo affermare che lo sviluppo della disfagia può essere strettamente legato alla presenza di neoplasie riguardanti il distretto testa collo e neoplasie del SNC.
Per ciò che riguarda lo stile di vita, vanno fatte importanti considerazioni poichè i fattori personali possono condizionare il quadro clinico complessivo e la risposta alle terapie. In ogni caso la concomitante presenza dei fattori di rischio rappresenta un elemento predisponente sia per l’insorgenza della disfagia, che per l’aggravarsi della stessa condizione clinica.
Ad esempio sia il tabagismo che l’alcolismo ricoprono un aspetto fondamentale poichè condizionano processi irritativi a livello della mucosa delle vie digestive e respiratorie. Lo stile di vita naturalmente influenza anche il livello della massa magra, del condizionamento motorio e cardiovascolare che a sua volta possono interferire con il meccanismo della deglutizione causando alterazioni funzionali.
A proposito del fattore legato al condizionamento fisico - cardiovascolare e più precisamente alla percentuale di massa magra del soggetto, è utile dire che questi rappresentano fattori che possono offrire supporto migliorando le risposte alla malattia. Purtroppo la sarcopenia rappresenta una delle più comuni conseguenze legate allo sviluppo di patologie tumorali.
La perdita di massa muscolare può interessare anche i distretti anatomici interessati nel processo di deglutizione. Nei casi in cui la sarcopenia è limitata alla muscolatura deglutitoria, non si può parlare di disfagia sarcopenica come accade nella SLA.
Nei casi di disfagia sarcopenica vera, se non viene effettuato un attento monitoraggio, la diagnosi può concludersi solo in seguito all’evidenza clinica di malnutrizione e cachessia.
Comorbilità
In caso di invasione neoplastica delle aree in esame o quando vi sono effetti collaterali della chemio/radioterapia, i fattori legati alla neoplasia si combinano con patologie in corso. Così il loro effetto si amplifica e parallelamente viene a risultare in aumento il rischio di disfagia per slatentizzazione o peggioramento di condizioni preesistenti.
Tra le comorbilità più note aventi effetto sulla deglutizione abbiamo:
- Malattie cerebrovascolari
- Patologie del sistema immunitario
- Malattie della giunzione neuro-muscolare
In ogni caso lo scenario delle comorbidità associate all disfagia è di ampio spettro, ma ritornando sul tema delle malattie cerebrovascolari, uno studio ha preso in esame i pazienti con ictus ischemico acuto provenienti da due grandi corti rappresentative (studio STROKE-CARD 2014-2019 e registro STROKE-CARD 2020-2022, entrambi con sede a Innsbruck, Austria). Questi pazienti sono stati analizzati per la presenza di disfagia al momento del ricovero ospedaliero attraverso i relativi esami clinici della deglutizione e le comorbidità sono state valutate utilizzando il Charlson Comorbidity Index (CCI).
I risultati hanno evidenziato che la disfagia è correlata ad una serie di patologie come l'ipertensione, la fibrillazione atriale, il diabete, l'infarto del miocardio, l'insufficienza cardiaca, le malattie arteriose periferiche, la grave malattia epatica cronica e quella renale. Le associazioni più significative con la disfagia hanno tuttavia evidenziato il diabete, la malattia arteriosa periferica, la malattia renale e la malattia epatica.
Sempre in riferimento alle malattie ed agli eventi di carattere cerebrovascolare un altro studio che ha relazionato la disfagia nei pazienti con ictus ischemico, ha ritenuto fondamentale valutare la relazione tra disturbi della deglutizione e indicatori demografici e clinici selezionati. Sulla base dell'analisi della documentazione medica, sono stati identificati i parametri clinici più importanti, tra cui dati demografici, frequenza dei fattori di rischio di ictus, posizione della lesione ischemica, coinvolgimento corticale, gravità dell'ictus misurata dal NIHSS (Nationale Institutes of Health Stroke Scale) e metodi di alimentazione dei pazienti post-ictus. E’ importante sottolineare che la disfagia è stata osservata nel 65,9% dei pazienti nel gruppo di studio. Anche l'ipertensione è stata classificata come la malattia cronica più comune nella popolazione studiata di pazienti con ictus ischemico (91,8% dei pazienti). Nei pazienti con disfagia confermata è stato necessario apportare modifiche sostanziali alla tipologia di dieta ed in questo frangente, il fattore età ha giocato un ruolo significativo. In cocnlusione, l'identificazione precoce delle difficoltà di deglutizione nei pazienti con ictus è fondamentale per determinare un piano di alimentazione appropriato e sicuro, nonché per iniziare la terapia logopedica per migliorare l'efficacia della deglutizione e ridurre al minimo le complicazioni polmonari.
Età
E’ chiaro che bisogna anche focalizzare la visione su un organismo che invecchia dal punto di vista fisiologico. Con l’invecchiamento è probabile che si manifestino alterazioni funzionali legate ai processi fisiologici della deglutizione. Inoltre sono da considerare le alterazioni legate alle modificazioni anatomiche della colonna vertebrale, la riduzione dell’elasticità dei muscoli in generale, ridotta elevazione laringea ed ipostenia. Il fatto che spesso ci sia una perdita di controllo del sistema nervoso centrale, in concomitanza con altri fattori legati ai seni piriformi può determinare presbifagia,
che è la forma di disfagia connessa con i processi fisiopatologici dell’invecchiamento.
4.1 Trattamenti oncologici
La disfagia è una possibile conseguenza nei pazienti che vengono sottoposti a trattamenti per tumore testa collo. Tuttavia anche gli interventi chirurgici del complesso maxillo facciale possono avere il loro impatto, così come gli interventi di neurochirurgia. L’assunzione di farmaci e la radioterapia per i tumori testa collo, possono causare disfagia, determinando ritardi nella deglutizione, tosse o soffocamenti e dolore durante la deglutizione.
Gli interventi alla faringe ed alla laringe invece, possono causare difficoltà del passaggio di liquidi dalla bocca all’esofago.
4.2 Chirurgia
La disfagia post estubazione è un elemento spesso sottovalutato ma è da ricordare che riguarda una buona percentale dei pazienti sottoposti ad interventi chirurgici, i dati parlano dal 3% al 60% dei soggetti intubati.
L’intubazione dunque può causare disfagia ma questa è reversibile nei casi in cui la stessa intubazione risulta temporanea e di breve durata. La lesione è caratterizzata da un meccanismo che riguarda il danneggiamento di protezione delle vie aeree. Chiaramente questi effetti possono risultare maggiormente marcati in caso di alterazioni sensoriali cognitive, reflusso gatro-esofageo ed effetti collaterali di alcuni farmaci come detto prima, che risulta deleterio per i normali meccanismi di deglutizione. Alcuni di questi farmaci includono Morfina e Midazolam.
Ricerche mirate studiano il legame tra respirazione e deglutizione. Infatti in fase di post estubazione si è visto venire meno questo legame con conseguenti alterazioni del meccanismo, ecco perchè si parla di polmonite ab-ingestis. Le vie aeree superiori si possono ledere durante i tempi di intubazione che superano le 48 ore così come la presenza di una via aerea artificiale e di cicli prolungati di ventilazione.
L’utilizzo di nuove tecnologie non invasive hanno in ogni caso migliorato la comprensione del profondo legame che esiste tra il meccansimo della deglutizione e quello della respirazione.
4.3 Chemioterapia
Le terapie antiblastiche portano molto spesso disturbi del cavo orale come le mucositi dell’esofago e del tratto gastroenterico, si stima che il dato possa interessare un alto numero di pazienti sottoposti a questo tipo di trattamenti. I farmaci che possono ricondurre ai disturbi sono: le fluoropirimidine, le antracicline, gli antimetaboliti ed i taxani, utilizzati in numerosi tumori. Altre terapie a base di farmaci potenzialmente interessati nella produzione di gravi effetti collaterali sono cisplatino oppure carboplatino, 5 Fluorouracile, cetuximab ed i farmaci immunologici . Tra questi, gli inibitori EGFR causano mucositi. Questi farmaci causano disepitelizzazione, alterazioni dei nervi periferici ed incoordinazione della deglutizione.
Anche altri fattori tuttavia possono aggravare l’entità del quadro clinico: parliamo di malnutrizione, disidratazione, alterata secrezione salivare, cattiva igiene del cavo orale, ed assunzione cibi eccessivamente caldi e/o piccanti.
4.4 Radioterapia
La disfagia rappresenta una delle possibili condizioni di tossicità a cui il paziente va incontro nell’ambito dei trattamenti radioterapici, oltre che a molteplici deficit strutturali conseguenti al trattamento.Si può assistere anche a (xerostomia) o ispessimento della saliva, danni alla mucosa di rivestimento del cavo orale, gonfiore, dolore, ulcere, danneggiamento delle papille gustative. Tutto questo è naturalmente legato al rallentamento della guarigione oltre alle note modifiche ed alterazioni del gusto e tutti i relativi problemi a livello sensoriale. Anche la tiroide è un organo fortemente interessato nei trattamenti radioterapici proprio per il suo posizionamento dal punto di vista anatomico. L’alterazione delle funzioni della tiroide può causare numerosi sintomi tra cui stanchezza, senso di indebolimento generale e difficoltà nell’ideazione. Il meccanismo di tossicità è già innescato entro pochi minuti dall'irradiazione. Il tasso di proliferazione delle cellule staminali diminuisce e si sviluppa una progressiva degradazione epiteliale come conseguenza del danno da radiazioni accumulato. L'inizio della riepitelizzazione delle cellule normali dipende fortemente dai parametri del trattamento.
Uno degli effetti più dannosi dell'esposizione alle radiazioni è l'induzione di una produzione eccessiva di specie reattive dell'ossigeno e dell'azoto (ROS). In condizioni fisiologiche, le ROS agiscono come mediatori della comunicazione all'interno della cellula e facilitano la segnalazione tra altre cellule. L'attività è altamente regolata, perché una produzione eccessiva può danneggiare le proteine e la struttura cellulare, innescando disfunzioni o apoptosi. Le ROS sono regolate controllando qualsiasi produzione eccessiva tramite rimozione enzimatica. I mitocondri all'interno di una cellula sono i maggiori produttori di ROS in condizioni stabili (ad esempio, anione superossido), durante la generazione di ATP (adenosina trifosfato) nel complesso I e III della catena di trasporto degli elettroni. I mitocondri impiegano anche difese antiossidanti (ad esempio, superossido dismutasi, catalasi) che sono in grado di neutralizzare o ridurre le ROS in una forma meno tossica. Quando si verifica uno squilibrio tra specie reattive e le loro difese antiossidanti, si può assistere a stress cellulare e alla distruzione finale dei tessuti, chiamata danno ossidativo. Una comprensione degli effetti biomolecolari delle radiazioni sul decorso temporale della guarigione delle ferite e sulle risposte morfologiche dei tessuti sottostanti che precedono il danno da radiazioni migliorerà comunque le opzioni disponibili per il trattamento della disfagia. Ma gli effetti delle radiazioni ionizzanti che inevitabilmente intaccano anche i tessuti sani e che possono manifestarsi con un’entità più o meno grave, vengono associati al fattore temporale dal momento che si parla di radiotossictà tardiva nel momento in cui il fattore tempo determina la comparsa di determinati sintomi anche mesi dopo la fine del trattamento. La radioterapia curativa nei tumori testa collo richiede la somministrazione di radiazioni focalizzati in una piccola area tumorale. Oggi per fortuna grazie all’ausilio di nuovi apparecchi è possibile limitare l’insorgenza degli effetti collaterali della radioterapia concentrando il fascio di radiazioni sull’area interessata, limitando così i danni anatomici alle strutture circostanti. L’uso esteso di IMRT a intento curativo nella pratica clinica ha permesso un miglioramento degli esiti oncologici e una riduzione della tossicità legata alle radiazioni.
4.5 Effetti della radioterapia sui muscoli della deglutizione
In base al tipo di fibra e alla risposta ai ROS, i muscoli con la più alta capacità glicolitica (tipo IIB) sono maggiormente a rischio di danni da radiazioni. Ad esempio, lo strato esterno dei muscoli costrittori faringei inferiori negli esseri umani è prevalentemente composto da fibre di tipo II con una bassa capacità ossidativa rispetto allo strato interno. Pertanto, il distinto compartimento neuromuscolare esterno ritenuto responsabile del movimento grossolano del bolo attraverso il lume potrebbe essere a maggior rischio di danni da radiazioni. Clinicamente, i sopravvissuti a HNSCC irradiati spesso presentano difficoltà attribuite alla dismotilità faringea, tra cui un movimento del bolo compromesso durante la deglutizione e residui post-deglutizione nella parete faringea posteriore, nel vestibolo laringeo e nel seno piriforme.
Esistono diversi altri muscoli della deglutizione composti da fibre con elevata capacità glicolitica. Data questa conoscenza, forse non sorprende che diversi muscoli siano stati identificati come strutture critiche a rischio di causare disfagia post-radiazioni. Tuttavia, studiare questi tipi di fibre muscolari in isolamento non tiene conto delle differenze in altre proprietà fisiologiche, come l'influenza relativa che ogni muscolo esercita durante la deglutizione e lo spettro di muscoli con distribuzione eterogenea rispetto a quella omogenea del tipo di fibra. Inoltre, è noto che il danno ossidativo è altamente selettivo per le fibre di tipo II. Ciò si basa sul fatto che i mitocondri all'interno di ogni tipo di miofibra hanno caratteristiche intrinseche uniche che possono alterare l'elaborazione dei ROS. Come descritto in precedenza, i ROS sono un sottoprodotto della normale produzione di energia nei mitocondri e sono anche indotti durante la difesa immunitaria dell'ospite e in risposta alle radiazioni. Lo stress ossidativo può verificarsi quando c'è uno squilibrio tra i ROS e le difese antiossidanti. Alla luce della nostra limitata conoscenza dei muscoli faringei che sono vitali per la deglutizione funzionale e la protezione delle vie aeree, sono necessari ulteriori studi per caratterizzare i cambiamenti nelle richieste metaboliche e fisiologiche della diversa muscolatura coinvolta nella deglutizione, consentendo così un'ulteriore tassonomia dei muscoli maggiormente a rischio di danni da radiazioni.
Il TDRS è uno strumento che risulta utile per poter predire la disfagia nei pazienti sottoposti a trattamento radioterapico per i tumori testa collo, dopo circa sei mesi dall’inizio della terapia. Questo sistema tiene conto dell’estensione del tumore, dell’esatta localizzazione, la sua classificazione nonchè l’estensione dell’irradiazione.
E’ importante sottolineare che il risultato mostrerà un punteggio che includerà i valori relativi al calo ponderale del soggetto, individuando tre possibili livelli di rischio: 0-9 basso, 10-18 medio, >18 alto).(14,15).
Il rischio più alto va associato ai tumori della rinofaringe secondo cui si è registrato un calo ponderale del 10% prima dell’inizio della radioterapia e che abbiano richiesto una radioterapia accelerata bilaterale del collo.

5 Scelta degli alimenti
La modifica della consistenza è diventata una delle forme più comuni di intervento per la disfagia ed è ampiamente considerata importante per promuovere una deglutizione sicura ed efficiente. Tuttavia, ad oggi, non esiste una convenzione univoca per quanto riguarda la terminologia utilizzata per descrivere i livelli di addensamento dei liquidi o la modifica della consistenza del cibo per uso clinico. Ad ogni modo, c’è da dire che la maggior parte delle linee guida esistenti per la terminologia della consistenza sono state sviluppate sulla base di input derivati da opinioni di esperti, focus group e interviste con medici, inoltre alcune linee guida hanno attinto a prove dalla letteratura per supportare la loro nomenclatura .
Il progetto International dysphagia diet standardization initiative, come vedremo in seguito ha l'obiettivo di considerare le attuali prove empiriche quando si determina il numero e le caratteristiche dei termini che dovrebbero essere utilizzati in una tassonomia raccomandata di liquidi addensati e alimenti con consistenza modificata per uso clinico. Come primo passo verso la creazione di una tassonomia comune, è stata intrapresa una revisione sistematica per identificare prove empiriche che descrivono l'impatto della consistenza dei liquidi e della consistenza del cibo sul comportamento di deglutizione. Alla luce di ciò, sono state rivelate due tendenze chiave rispetto all'impatto dei liquidi addensanti sulla deglutizione: i liquidi più densi riducono il rischio di penetrazione-aspirazione, ma aumentano anche il rischio di residui post-deglutizione nella faringe. In ogni caso la letteratura riguardante gli studi non era sufficiente a supportare la delineazione di limiti di viscosità specifici o altre proprietà materiali quantificabili correlate ai risultati clinici. Per quanto riguarda la consistenza del cibo, la letteratura ha indicato proprietà di durezza, coesione e scivolosità come rilevanti sia per i comportamenti fisiologici che per i modelli di flusso del bolo, ed ha altresì suggerito la necessità di classificare il comportamento del cibo e dei fluidi nel contesto dei processi fisiologici coinvolti nel trasporto orale e nell'inizio del flusso.
Uno dei pilastri fondamentali che costituisce la pratica clinica per affrontare la disfagia è rappresentato dall’uso di cibi dalla consistenza modificata. Ci si basa sul criterio che fa riferimento alla sicurezza durante il processo di deglutizione modificando appunto la consistenza degli alimenti. Nel caso dei liquidi, è ampiamente accettato che i liquidi sottili (come l'acqua) pongono sfide di sicurezza non indifferenti per le persone affette da disfagia perché scorrono rapidamente. La velocità del flusso del bolo dalla bocca alla faringe può essere sufficientemente rapida da non fornire abbastanza tempo alla persona per chiudere le vie aeree prima che il bolo arrivi all'ingresso della laringe e delle vie aeree. In questo caso, i liquidi addensati sono raccomandati con l'obiettivo di rallentare il flusso dei liquidi per consentire più tempo per la chiusura delle vie aeree. Al contrario, liquidi molto densi e materiali alimentari solidi possono richiedere una maggiore forza in termini di forze propulsive della lingua che vengono utilizzate per guidare il materiale attraverso l'orofaringe. Se una persona ha una forza ridotta della lingua o una forza ridotta dei muscoli faringei, si ritiene che ciò costituisca un rischio per i residui di rimanere nei recessi della faringe dopo una deglutizione. Allo stesso modo, i cibi solidi che richiedono masticazione possono rivelarsi difficili per le persone con problemi dentali o debolezza nei muscoli masticatori. L'alterazione delle proprietà dei cibi solidi (tagliandoli a cubetti, tritandoli, tritandoli o frullandoli) è un approccio comune per rendere questi materiali più facili da elaborare e deglutire per via orale.
L'uso diffuso della modifica della consistenza come intervento clinico ha creato la necessità di stabilire una terminologia chiara per descrivere le consistenze target raccomandate per i pazienti con disfagia. In assenza di una terminologia e definizioni chiare per guidare sia la produzione/preparazione che l'uso clinico di consistenze alimentari modificate e consistenze liquide, diversi paesi hanno sviluppato tassonomie o sistemi di classificazione, diffusi sotto forma di linee guida cliniche. Tuttavia, diversi paesi hanno sviluppato sistemi di classificazione diversi. Il riconoscimento della necessità di concordare sulla terminologia sia all'interno che tra le giurisdizioni geografiche ha portato alla creazione dell'International Dysphagia Diet Standardisation Initiative. La task force IDDSI si è posta l'obiettivo di sviluppare una terminologia e definizioni standardizzate globali per alimenti con consistenza modificata e liquidi addensati per individui con disfagia di tutte le età, in tutti gli ambienti di cura e in tutte le culture.
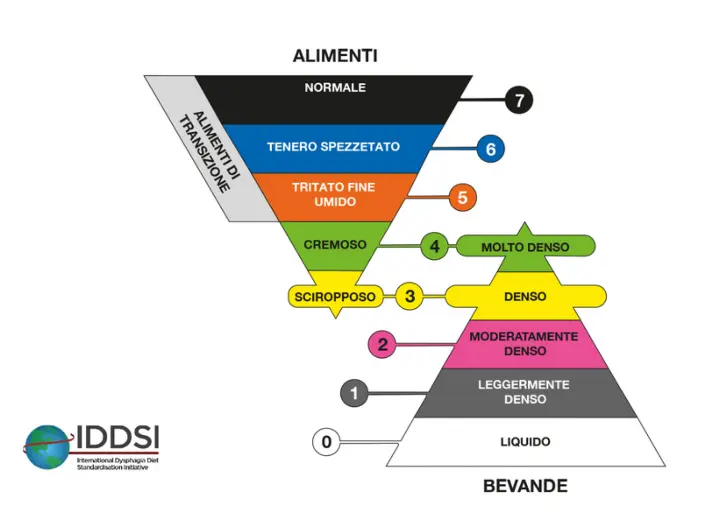
5.1 La IDDSI ( International dysphagia diet standardization initiative)
L’Iniziativa Internazionale per la Standardizzazione della Dieta in Disfagia (IDDSI) nasce nel 2013 con il fine di creare, a livello mondiale, un nuovo lessico standard e delineare le “texture” degli alimenti modificati e degli addensati, per persone con disfagia, nelle diverse età, contesti di cura e culture.
La piramide della disfagia
A seguito di tre anni di lavoro, il Comitato internazionale per la standardizzazione della dieta in disfagia creò nel 2016 e pubblicò nel 2017, un diagramma fatta da una piramide di 8 livelli. I livelli sono identificati da numeri, etichette di testo, e codici colore.
Il sistema IDDSI è formato da un continuum di 8 livelli (0 - 7), in cui le bevande sono valutate con i livelli 0 - 4, e gli alimenti sono valutati con i livelli 3-7. Il framework IDDSI offre un lessico comune per descrivere le consistenze alimentari e lo spessore dei liquidi. Le metodologie di test IDDSI sono concepite per verificare il flusso o i tratti di consistenza di un prodotto specifico all'atto del test, da svolgere su cibi e liquidi nelle condizioni di somministrazione attese (specialmente la temperatura). Al sanitario compete la responsabilità di dare indicazioni per cibi o liquidi a un paziente specifico, basandosi sulla sua completa valutazione clinica. Il Quadro IDDSI contempla l'impiego di un lessico standardizzato allo scopo di descrivere le consistenze alimentari e dei liquidi addensati, e i metodi di Valutazione (IDDSI TESTS) sono utili per stabilire il flusso o i tratti di consistenza di un dato prodotto all'atto del test, eseguito in seguito alla valutazione clinica per quel dato paziente.
Test di flusso: è un metodo utilizzato per valutare la consistenza dei liquidi addensati, in modo da garantire che siano adatti per le persone con disfagia. Questo test misura quanto liquido rimane in una siringa dopo un certo periodo di tempo, avendola prima riempita appositamente con una quantità di 10 ml, permettendo di determinare la sua densità ed è suddiviso in cinque diverse fasi. Nella fase di preparazione si riscalda il liquido alla temperatura prevista per il consumo; il versamento prevede che venga versato il liquido in una siringa; tempo di Flusso lasciando che il liquido fluisca per 10 secondi; misurazione dopo 10 secondi per misurare il livello del liquido rimasto nella siringa; infine la Valutazione in cui si confronta il livello del liquido con le linee guida IDDSI per determinare la consistenza appropriata (ad esempio, denso, moderatamente denso, leggermente denso, liquido, ecc.
Prima di procedere è importante controllare la lunghezza della siringa perchè ci sono siringhe di lunghezza differente.
Metodi di analisi degli alimenti
Vengono forniti i classici utensili da cucina ovvero forchette e cucchiai utilizzati singolarmente oppure in combinazione, che oltre ad essere poco costosi appaiono utili in questo caso per ridurre il rischio di soggettività legato a questo genere di test. Il test di gocciolamento della forchetta, il test di inclinazione del cucchiaio, il test di pressione della forchetta o del cucchiaio, il test della bacchetta e il test del dito vengono utilizzati per testare sia cibi morbidi che solidi.
Fork Drip Test
Il Fork Drip Test viene utilizzato per verificare il corretto spessore e la coesione degli alimenti di Livello 3-5, valutando se scorrono o come rimangono uniti nelle fessure/punte di una forchetta e confrontandoli con le descrizioni dettagliate di ciascun livello.
Test di inclinazione del cucchiaio
Il test dell'inclinazione del cucchiaio viene utilizzato per determinare l'appiccicosità degli alimenti (adesività) e la capacità degli alimenti di rimanere uniti (coesività).
Test di pressione della forchetta e test di pressione del cucchiaio
Per verificare quanto è duro o sodo un alimento, il test di pressione della forchetta è il metodo migliore per valutare gli alimenti nei livelli 4 - EC7 e gli alimenti di transizione, valutando come cambia l'alimento quando si applica pressione con i rebbi/punte di una forchetta o il dorso di un cucchiaio. Le fessure/spazi tra i rebbi/punte di una forchetta di metallo standard misurano in genere 4 mm, il che fornisce un utile strumento di misurazione per la dimensione delle particelle degli alimenti al livello 5 - Tritato e umido. In questo contesto è importante notare che la dimensione delle particelle è diversa per i bambini piccoli.
Test delle bacchette
Se non si hanno a disposizione le forchette, si possono usare le bacchette per raccogliere e spezzare il cibo e determinarne le caratteristiche e il comportamento.
Test delle dita
I test delle dita sono stati incorporati nel riconoscimento che questo potrebbe essere il metodo più accessibile in alcuni paesi.
5.2 Consistenze degli alimenti
Livello 0: liquidi aventi consistenza simile all’acqua.
Defluiscono velocemente e che possono essere bevuti con qualsiasi tipo tazze o cannucce, come più opportuno in relazione alle abilità. Questa tipologia richiede la capacità funzionale di gestire ogni tipo di liquido in sicurezza.
Livello 1: poco denso o leggermente denso rispetto all’acqua
Sforzo minimo nel bere rispetto al liquido di livello 0. Presenta una consistenza analoga ai preparati anti-rigurgito per neonati, reperibili sul mercato, e trova impiego primario in ambito pediatrico quale bevanda densificata a lento scorrimento. È possibile il suo utilizzo negli adulti se occorre diminuire il ritmo di deglutizione di una bevanda.
Livello 2: moderatamente denso.
Defluisce dal cucchiaio con minor velocità di un liquido livello 0-1. È sorseggiabile ma necessita più impegno dei gradi precedenti se bevuto tramite una cannuccia comune. Quando i liquidi di livello più basso sono deglutiti troppo celermente e non in modo sicuro, questa densità scorre appena più lenta e potrebbe essere adatta se il controllo linguale è un po' più limitato.
Livello 3: sciropposo denso.
Si può ingerire col cucchiaio senza bisogno di masticare; infatti, cibi di tale densità sono inghiottiti direttamente, avendo una tessitura uniforme, senza grumi, pezzi di guscio, bucce, pelle, cartilagini o ossa. Si può consumare da una tazza e implica una certa fatica se ingerito tramite cannuccia comune (con diametro di 6.9 mm). Se versato in un piatto, perde coesione e non si può mangiare con la forchetta dato che cola piano tra i denti della stessa. Se colato dal cucchiaio, lascia pochissimo residuo. Questo genere di densità è consigliata se c'è un controllo linguale carente con liquidi meno densi (fino al Livello 2) e permette un tempo più lungo per la gestione orale. Però, necessita di una certa spinta della lingua ed è appropriato in caso di deglutizione dolorosa.
Nel test di scorrimento, il campione liquido passa in una siringa da 10 ml in ≤ 10 secondi, con un residuo > 8 ml; cola lentamente tra i denti di una forchetta e la sua traccia non forma un disegno definito sulla superficie. Su una superficie orizzontale, si allarga e, dopo la pressione della forchetta, non mantiene la compattezza. L'uso delle bacchette è sconsigliato per tale densità e non si riesce a trattenere una piccola quantità di cibo sul dito, dato che questa densità fa scivolare il cibo facilmente dalle dita, lasciando solo tracce minime. Appartengono al Livello 3: cibi per neonati (creme di riso/semolini allungate, mousse di frutta allungate, etc.), certi tipi di salse e condimenti secondo il test di flusso IDDSI, determinati sciroppi, latte concentrato, ecc.
Livello 4: cremoso / molto denso.
I suoi tratti distintivi implicano che di norma si consumi col cucchiaio (fattibile pure con la forchetta) però non è possibile berlo. Non si può aspirare mediante cannuccia tuttavia non necessita di essere masticato. Conservando la sua forma, si nota lo slittamento che si verifica piano sotto l'azione gravitazionale, ma non è possibile versarlo. È esente da grumi, non risulta colloso e non si scompone dal componente solido. La base fisiologica per questa densità specifica stabilisce un utilizzo riservato quando la mobilità della lingua è molto limitata, oppure in caso di protesi dentaria non funzionante e nei casi di masticazione con dolore. Implica inoltre un impegno propulsivo del bolo inferiore a quello del tritato fine/umido (Livello 5), del Tenero Spezzettato (Livello 6), del Facilmente Masticabile (Livello 7), ma più gravoso se paragonato allo Sciropposo (Livello 3). Un ulteriore tratto che definisce la tipologia del livello 4, palesa che non è necessario l'atto del "mordere" né la masticazione e non si contempla la creazione del bolo. Per questa situazione la prova di flusso non si può applicare; infatti, si adotta quella della forchetta o, come opzione diversa, la prova del cucchiaio reclinato. Nel corso della prova di pressione con la forchetta il campione mantiene la sua traccia. Durante la prova di gocciolamento, l'alimento si accumula sopra la forchetta, creando una piccola altura, e una quantità limitata di esso può passare tra i rebbi formando un'estensione che non cola né gocciola. Nella prova del cucchiaio reclinato appare coeso, mantiene la propria forma al suo interno, però precipita dal cucchiaio inclinato o tenuto “di taglio” con un impercettibile movimento di quest'ultimo. L'assaggio di cibo slitta via agevolmente, rilasciando un velo sottile e trasparente attaccato al cucchiaio; comunque sia, non si dimostra né colloso, né compatto e non ha la capacità di distendersi lievemente sopra un piatto piano.
Non è fattibile esaminare un campione di tale densità adoperando le dita. La sua "trama" consente uno slittamento agevole, depositando residui minimi fra le dita (sottile velo).
Livello 5: tritato fine e umido.
Questo alimento si consuma con forchetta o cucchiaio; le bacchette sono possibili solo con eccellente controllo manuale. Si presenta modellabile, soffice, umido, privo di liquidi separati, con piccoli grumi interni facilmente comprimibili con la lingua. I grumi devono misurare per i bambini ≤2mm (larghezza) x ≤8mm (lunghezza), mentre per gli adulti ≤4mm (larghezza) x ≤15mm (lunghezza). Non è necessario mordere, ma è richiesta una minima capacità masticatoria e sufficiente forza linguale per la gestione del bolo. È una consistenza indicata in caso di masticazione dolorosa, affaticamento, assenza di denti (edentulia) o protesi dentali inadeguate.
Durante il test di pressione con la forchetta, le particelle dell'alimento si dividono e possono passare attraverso i rebbi, senza tuttavia che vi sia scorrimento di liquido; il cibo è facilmente comprimibile esercitando una minima pressione (senza che l'unghia del pollice sbianchi). Nel test del cucchiaio inclinato, il campione di cibo mantiene la propria forma sul cucchiaio e scivola via in blocco se il cucchiaio viene inclinato o scosso lievemente, lasciando un residuo esiguo e non risultando colloso; può espandersi un poco se versato su un piatto. È possibile manipolare un campione di questa consistenza tra le dita: piccole particelle morbide, umide e lisce possono essere schiacciate, lasciando le dita bagnate.
Alimenti tipici includono: tritati fini o sminuzzati (carne, pesce) ai quali si può aggiungere salsa o sugo omogeneo per amalgamare (lo spazio tra i rebbi di una forchetta può aiutare a verificarne correttamente le dimensioni). La frutta deve essere tritata, finemente grattugiata oppure schiacciata, eliminando eventuali liquidi in eccesso; è possibile aggiungere crema, panna o mousse per amalgamare, rispettando le dimensioni dei grumi indicate. I cereali si presentano in preparazioni dense con piccoli grumi soffici, con una consistenza simile a quella di una zuppa densa ma senza liquidi in eccesso. Il pane è generalmente sconsigliato, ad eccezione di pane bianco da toast o pan-brioche (privati della crosta) sbriciolato, imbevuto di latte o brodo e poi ricomposto, amalgamato con salse cremose. Riso, couscous e quinoa devono essere ben cotti, compatti, non sgranati e non appiccicosi, conditi con salse, panna o sughi cremosi senza eccessi liquidi.
Il cibo di questo livello deve superare tre test fondamentali
Test dei rebbi della forchetta: per determinare la dimensione dei grumi, che deve rispettare i parametri sopra indicati per bambini e adulti
Test della pressione con la forchetta: il cibo deve risultare morbido e soffice, tanto da essere schiacciato facilmente senza che la pressione provochi lo sbiancamento dell'unghia del pollice
Test del cucchiaio inclinato: il campione di cibo deve mantenere la sua forma sul cucchiaio e cadere abbastanza facilmente se il cucchiaio viene inclinato o leggermente scosso, senza risultare solido o appiccicoso.
Livello 6: tenero spezzettato
Benché la masticazione sia imprescindibile, l'atto del mordere non è richiesto per questa tipologia di alimenti. Tale consistenza è indicata in situazioni di dolore o affaticamento durante la masticazione, in caso di mancanza di denti (edentulia) o qualora le protesi dentarie non siano perfettamente funzionanti, poiché sono necessarie una buona forza e un adeguato controllo linguale per gestire il cibo nelle fasi di masticazione e successiva deglutizione. La grandezza dei frammenti alimentari, che deve essere proporzionata all'età e alle capacità del soggetto (non eccedendo gli 8 mm per i bambini e 1,5 cm per gli adulti), è studiata per ridurre al minimo il rischio di soffocamento.
Questo cibo, caratterizzato da una tessitura soffice e tenera, priva di componenti a doppia consistenza, si può consumare agevolmente con la forchetta, il cucchiaio o, in certi casi, con le bacchette. L'uso del coltello non è necessario per porzionarlo, essendo sufficienti gli stessi utensili da tavola.
Le verifiche di cedevolezza dimostrano la sua natura: un campione di circa 1,5 cm x 1,5 cm (paragonabile all'unghia di un pollice), se sottoposto a pressione con la base della forchetta, il dorso del cucchiaio, o tra pollice e indice (fino a causare lo sbiancamento delle unghie), si deforma, si disgrega e non recupera la sua forma originaria una volta che la pressione cessa. È importante notare che sia la forchetta che il cucchiaio, utilizzati di taglio, possono servire a ridurre ulteriormente il cibo in pezzi più piccoli.
Livello 7: facilmente masticabile
Questo livello di consistenza definisce la capacità di mordere cibi teneri e masticare per formare un bolo coeso e morbido pronto per essere deglutito, pur non richiedendo necessariamente i denti. Implica la facoltà di masticare e aggregare il bolo senza eccessivo affaticamento, risultando adatto a persone con masticazione e deglutizione difficoltosa verso alimenti che potrebbero causare soffocamento, specie in pazienti con rischio già identificato. Tale consistenza alimentare può trovare impiego nella riabilitazione deglutitoria sotto controllo logopedico e se esistono abilità masticatorie più avanzate. Importante notare che il livello 7 esclude pezzetti duri, semi, bucce, parti fibrose di frutta/verdura, lische, nonché elementi fibrosi, gommosi, cartilaginei, croccanti o friabili. Può, però, includere cibi e liquidi a consistenza mista, se vi è sicurezza clinica per il Livello “0”; altrimenti, la componente liquida andrà addensata su indicazione clinica. Si tratta di alimenti comuni di consistenza tenera, adeguati allo sviluppo evolutivo e all'età.
Cibi sottoposti a test di pressione della forchetta
Per l'assunzione di questi alimenti, ogni strumento, come posate o bacchette, può essere usato a piacere. Non ci sono restrizioni dimensionali assolute per il livello 7, ma si suggeriscono pezzetti intorno agli 8 mm per i bambini, mentre per gli adulti sono indicati frammenti di circa 1.5 cm.
Infine, la supervisione durante i pasti può essere necessaria per individui ad alto rischio con problemi di masticazione/deglutizione che adottano comportamenti non sicuri. Le raccomandazioni cliniche in ogni caso ritengonio indispensavile una consulenza deglutologica.
Sul test di pressione della forchetta il campione, di dimensione pari a ~1.5 cm x 1.5 cm, risulta deformabile quando si preme fino a che l’unghio diventi bianco. Non ritorna nella sua forma originale. All pressione del cucchiaio si deforma senza riprende forma originale. Nel delle dita il campione si frantuma e non riprende la propria forma iniziale.
Cibo normale:
Sono richieste precise abilità per gestire questo livello: la capacità di masticare a lungo cibi di ogni possibile consistenza, trasformandoli in un bolo morbido e coeso, nonché quella di processare tutte le texture senza incorrere in affaticamento. Si aggiunge a ciò la competenza nel riconoscere, rimuovere ed espellere dalla bocca le parti non ingeribili, come ad esempio ossa, frammenti di cartilagine o lische di pesce.
Sono contemplate le “doppie consistenze” così come preparazioni definite “a consistenza mista”; sono inclusi alimenti duri, che presentano grumi, fibrosi, che risultano filanti, secchi, croccanti, inclini a sbriciolarsi o a frammentarsi, oltre a semi, pelli, bucce e cartilagini. Sebbene non esistano limitazioni specifiche per quanto concerne la dimensione e la forma dei bocconi, si suggeriscono pezzetti di grandezza prossima agli 8 mm (variabili) per i bambini, mentre per gli individui adulti sono più appropriati quelli di circa 15 mm, ossia 1.5 cm (variabili). Questi cibi, che spaziano da consistenze dure e croccanti a quelle più tenere, possono essere assunti con qualsiasi tipo di posata. In sostanza, questo livello designa il cibo con una consistenza considerata normale, vale a dire gli alimenti quotidiani che offrono diverse tessiture, in armonia con lo stadio di sviluppo e l'età della persona.
Cibi di transizione
I cibi di transizione, definiti dal framework IDDSI, sono alimenti aventi una texture iniziale (es. solida) che si modifica significativamente per azione di fattori esterni quali l'umidità (saliva, acqua) o variazioni di temperatura (riscaldamento, scioglimento). Questa trasformazione li rende più morbidi e gestibili, passando da una consistenza che può richiedere un minimo impegno masticatorio a una più facilmente frantumabile con la lingua. Il razionale fisiologico per il loro impiego in caso di disfagia si basa sulla capacità di stimolare gradualmente le abilità oromotorie e masticatorie, agendo da ponte verso alimenti più complessi senza necessitare di una vera e propria abilità di mordere. Richiedono poca capacità di masticazione iniziale, ma il paziente deve possedere un controllo orale sufficiente per gestire la texture in evoluzione e prevenire l'aspirazione, specialmente se il cibo si disintegra in una forma liquida. La classificazione di un alimento come "di transizione" è rigorosamente determinata dai test IDDSI, come quello di pressione della forchetta nell’immagine precedente o del cucchiaio dopo umidificazione, che verificano la deformabilità e la perdita della forma originale: il campione deve facilmente sformarsi e non ritornare alla sua forma iniziale, oppure dissolversi. Esempi comuni includono specifici wafer o biscotti che si ammorbidiscono rapidamente, alcuni snack soffiati, gelati o ghiaccio. Questi alimenti possono essere preziosi nei piani riabilitativi, sia in ambito pediatrico che adulto (es. post-stroke), per incoraggiare la progressione della dieta, stimolare la funzione masticatoria e migliorare l'esperienza alimentare del paziente con disfagia, offrendo varietà sensoriale e motivazione.
5.3 Consistenze ad alto rischio di soffocamento
Numerosi rapporti autoptici internazionali evidenziano come la natura di certi cibi incrementi notevolmente il pericolo di soffocamento, giustificandone l'esclusione dalle scelte alimentari raccomandate dalle linee guida. Ad esempio, le consistenze dure e secche (come noci, carote crude, popcorn) e quelle croccanti (tipo pane secco, bacon croccante) richiedono un'efficiente masticazione e una buona imbibizione salivare per essere umidificate e deglutite in sicurezza. Analogamente, le tessiture fibrose (come la bistecca o l'ananas) necessitano di una masticazione prolungata per essere adeguatamente sminuzzate.
Un altro gruppo di alimenti problematici include quelli gommosi (certe tipologie di formaggio, marshmallow, purè eccessivamente denso) e quelli appiccicosi (come il burro di arachidi o caramelle gelee), poiché possono aderire alle mucose orali ed essere inalate. Anche le forme rotonde o allungate (uva, piccole salsicce), se non ben masticate, possono ostruire le vie aeree. Similmente, le consistenze sottili e flessibili (foglie di insalata) possono, se non masticate, occludere il passaggio dell'aria. Le croste e le parti abbrustolite (fritture, esterno degli arrosti) esigono una buona capacità masticatoria.
Consistenze friabili invece (biscotti secchi, grissini) domandano un ottimo controllo linguale per amalgamare i frammenti con la saliva in un bolo coeso. Pericoli possono derivare anche da semi, bucce e cuticole vegetali (semi di mela, buccia dei legumi), spesso duri, fibrosi o appuntiti, che necessitano di efficace triturazione e insalivazione, o di essere espulsi. Ossa e lische, chiaramente, richiedono abilità linguali per la loro rimozione.
Infine, le preparazioni a consistenza mista (latte con cereali, minestrone) o complessa (panini farciti, pizza), così come gli alimenti succosi dove il liquido si separa dal solido (anguria), pongono sfide significative, richiedendo la capacità di gestire simultaneamente o sequenzialmente componenti diverse. Anche le tessiture filamentose (fagiolini) possono creare difficoltà, poiché i filamenti possono rimanere intrappolati
Una domanda interessante che emerge da diversi studi e dalla letteratura che abbiamo oggi a disposizione, è se gli stimoli di consistenza della pasta adesiva come la crema di formaggio o il burro di arachidi debbano essere considerati alimenti semisolidi o liquidi estremamente densi. Questi elementi possono essere compressi e distribuiti sul palato con la lingua e non si fratturano; in quanto tali, in senso fisiologico, si comportano in modo abbastanza diverso e comportano comportamenti di elaborazione orale diversi dagli alimenti che richiedono masticazione. D'altra parte, non scorrono né per gravità né sotto le tipiche pressioni applicate dalla lingua e richiedono la manipolazione da parte della lingua per il trasporto attraverso la cavità orale, a questo proposito, sono abbastanza diversi dai liquidi. Pertanto, le definizioni fisiologiche di consistenza potrebbero avere confini diversi per diversi gruppi di consumatori. Le considerazioni sulla temperatura all'interno della bocca e sulla scivolosità delle superfici orali, date le differenze nei livelli di saliva durante la durata dell'elaborazione orale, sono senza dubbio rilevanti anche per lo sviluppo di un sistema di classificazione della consistenza per la popolazione disfagica, che si basa su un quadro fisiologico.
5.4 Aspetti clinici sulla consistenza degli alimenti
Da una prospettiva clinica, vi è una mancanza di indicazioni riguardanti la classificazione, l'etichettatura e la preparazione di alimenti dalla consistenza modificata per le persone con disfagia e questo aspetto rappresenta senz’altro una forte preoccupazione. Non è raro infatti che le indagini del medico legale su episodi di soffocamento fatali in persone a rischio di disfagia concludano che è stato ingerito cibo di consistenza inappropriata. Un recente rapporto della Commissione giapponese per la sicurezza alimentare ad esempio, specifica che la consistenza del cibo (levigatezza della superficie, elasticità, durezza), le dimensioni e la forma sono tutte rilevanti rispetto al rischio di soffocamento. Nelle loro indagini, si è scoperto che le torte di riso glutinoso sono la causa principale di incidenti di soffocamento, ma anche le tazze di gelatina sono state menzionate come una causa non infrequente di soffocamento. Il rapporto sottolinea che il rischio di soffocamento con un particolare alimento deve essere compreso sia in termini di proprietà di consistenza del bolo sia di comportamenti fisiologici comunemente utilizzati durante l'ingestione di tale alimento. Pertanto, le coppette di gelatina, per le quali descrivono un comportamento comune di inclinazione della testa all'indietro per succhiare la gelatina dalla coppetta, non sono esenti da rischi. Sulla base dell'attuale revisione, si è obbligati a sottolineare che le migliori prove disponibili riguardanti la selezione di una consistenza alimentare ottimale per una persona con disfagia derivano dall'attenta esplorazione della tolleranza per diversi alimenti in una valutazione clinica completa della deglutizione. Le revisioni sistematiche hanno rilevato una mancanza di prove di ricerca che forniscano supporto per la selezione o l'evitamento di consistenze specifiche, per questo motivo è indicata l'urgente necessità di generare prove empiriche per descrivere diverse classi di alimenti masticabili, in modo che possano essere definite le corrispondenti differenze previste nell'elaborazione orale e nel comportamento di deglutizione. Inoltre, lo sviluppo di metodi validi per osservare, descrivere e misurare i comportamenti della fase orale durante le attività di valutazione che sondano una varietà di diversi alimenti solidi sarebbe una preziosa aggiunta agli attuali metodi clinici soggettivi. In ogni caso le diverse prove che gli studi hanno fin’ora fornito, mostrano un beneficio associato all'addensamento dei liquidi in termini di riduzione della penetrazione e dell’aspirazione, d’altra parte questo beneficio comporta un rischio di residui post-deglutizione nella faringe con consistenze più dense.
Le potenziali delineazioni con utilità clinica includono la differenziazione dei liquidi in quelli che scorrono facilmente nel contesto di pressioni minime della lingua applicate in bocca rispetto a quelli che richiedono un movimento della lingua più attivo per avviare il flusso. Il comportamento di un bolo nel contesto del contenimento del bolo, del movimento attivo della lingua o della masticazione (ad esempio, diffusione vs flusso vs frattura) può essere un altro modo utile per catturare proprietà clinicamente rilevanti della consistenza del cibo per la deglutizione e sembra anche essere rilevante in termini di rischio di soffocamento. Queste speculazioni sollevano l'intrigante possibilità che possano essere necessari diversi confini di consistenza e flusso del bolo per diverse sottopopolazioni all'interno del più ampio gruppo di consumatori clinici di persone con disfagia, a seconda delle loro capacità fisiologiche. Ad ogni modo è doveroso ribadire che il campo della disfagia è ancora relativamente agli inizi. Dato l'uso prevalente di alimenti con consistenza modificata e liquidi addensati nel trattamento della disfagia, è opportuno che le lacune in determinate aree di interesse vengano identificate e forniscano solide basi per una ricerca clinicamente rilevante per guidare le migliori pratiche.
5.5 Addensanti
Gli addensanti alimentari sono sostanze aggiunte agli alimenti per aumentarne la viscosità e migliorarne la consistenza senza alterarne il gusto. Sono utilizzati in una vasta gamma di prodotti alimentari, tra cui salse, zuppe, creme e bevande, per conferire una texture più densa e uniforme. Funzionano interagendo con le molecole d'acqua presenti negli alimenti, formando una rete tridimensionale che aumenta la viscosità. Questo può essere ottenuto attraverso diversi meccanismi come la gelificazione, l'associazione di molecole idrofile e idrofobe, o la formazione di complessi polimerici. Le interazioni chimiche favorite dall’addensante alimentare riguardano in primo luogo l’idratazione delle molecole, sappiamo infatti che sono idrofili il che significa che attirano e trattengono le molecole d'acqua. Quando vengono aggiunti agli alimenti si legano quindi all'acqua formando strutture di idratazione che aumentano la viscosità. Alcuni addensanti, come la pectina e l'agar-agar, formano gel in presenza di determinate condizioni, come il pH o la presenza di ioni metallici (es. calcio). Questi gel intrappolano l'acqua in una rete tridimensionale, aumentando la consistenza dell’alimento da somministrare. Alcuni prodotti che rientrano in questa categoria hanno la facoltà di interagire con le proteine presenti negli alimenti, in questo modo viene a formarsi una serie di complessi denominati proteine-addensanti che aumentano la viscosità e la stabilità dell’alimento.
Una particolare caratteristica degli addensanti rientra nell’effetto sospensione: in pratica possono mantenere le particelle solide in sospensione nei liquidi, prevenendo la separazione delle fasi e migliorando la texture dell’alimento.
Amidi modificati ad esempio rientrano in questa categoria: sono derivati principalmente da mais, patate o tapioca, gli amidi modificati sono trattati chimicamente o fisicamente per aumentarne la solubilità e la stabilità. Esempi comuni includono l'amido ossidato e l'amido di mais modificato. Un altro noto addensante è rappresentato dalla gomma di Guar, un polisaccaride naturale estratto dalla pianta di Guar, utilizzato per addensare salse, zuppe e prodotti da forno. La gomma di Xantana invece è un polisaccaride prodotto da batteri, utilizzato per addensare bevande, salse e prodotti da forno. La Pectina
invece un polisaccaride naturale estratto dalle bucce degli agrumi, utilizzato principalmente nelle marmellate e gelatine.
L’ Agar-agar invece è un gelificante derivato dalle alghe marine, utilizzato in prodotti vegetariani e senza glutine.
Nella pratica clinica, gli addensanti sono spesso utilizzati per aiutare i pazienti con disfagia a consumare liquidi e alimenti in modo sicuro. Modificando la consistenza dei liquidi infatti, si riduce il rischio di aspirazione nei polmoni, prevenendo complicazioni come la polmonite ab ingestis che abbiamo precedentemente esaminato.
Gli addensanti vengono spesso prescritti dai medici o dagli specialisti in nutrizione per i pazienti con disfagia. La scelta di questa classe di prodotti e della loro concentrazione dipende dalla gravità della disfagia e dalle esigenze specifiche del paziente. È importante comunque seguire le indicazioni del medico per garantire che i liquidi siano addensati alla densità corretta per prevenire l’aspirazione. L’influenza degli addensanti si riflette sui diversi livelli di spessore e sulle dimensioni delle particelle nei boli alimentari, Nell’assistenza medica e infermieristica vengono utilizzati per rendere il cibo sicuro per i pazienti con disfagia.
Tuttavia l'effetto degli addensanti sugli alimenti a cui vengono aggiunti, in particolare durante la deglutizione, non è ancora chiaro, infatti come abbiamo accennato nel precedente paragrafo, l’argomento in questione necessita di ulteriori studi clinici al fine di mettere in luce le attuali lacune. Recenti studi mostrano che sono state fotografate le particelle del bolo di 20 volontari sani e le immagini digitali sono state utilizzate per stimare le dimensioni delle particelle in esse contenute. Sono stati testati otto campioni di prova con addensanti con diversi livelli di spessore: sei gradi di succo di carota addensato con carote crude, carota cruda con banana e carota cruda da sola. Sono stati calcolati l'indice di omogeneità delle particelle (HI) e l'indice di dimensione delle particelle (SI) appena prima della deglutizione. Sono state misurate anche le viscosità della parte liquida dei campioni di prova. Il numero di cicli di masticazione nei campioni di prova non era significativamente diverso. Tuttavia, sono state riscontrate differenze significative in SI e HI nei campioni di prova: i valori assoluti di SI e HI tendevano ad aumentare all'aumentare dello spessore del campione di prova ed anche la viscosità della parte liquida del campione di prova, aumentava significativamente all'aumentare dello spessore. Le differenze nello spessore del cibo avevano un'influenza sulle dimensioni delle particelle del bolo appena prima della deglutizione.
Per concludere, le prove disponibili fino ad oggi non ci aiutano a stabilire quanto grande debba essere una differenza di viscosità, per avere un effetto benefico e misurabile rispetto alla riduzione della penetrazione-aspirazione, né a che punto il rischio di accumulo di residui diventa una preoccupazione reale. Allo stesso modo, le prove disponibili non forniscono prove chiare per suggerire quanti livelli incrementali di viscosità crescente potrebbero essere significativi nel contesto clinico. I dati disponibili mancano anche di prove riguardo all'importante possibilità che proprietà di un bolo liquido come densità, stress di snervamento, coesione o scivolosità (per citarne alcune) possano influenzare la fisiologia e la funzione della deglutizione. Su quest'ultimo punto, siamo a conoscenza di una recente pubblicazione che descrive le differenze nei tassi di occorrenza della penetrazione-aspirazione per i liquidi, a seconda del tipo di addensante utilizzato (amido vs gomma di xantano), sebbene addensato a gradi diversi. Un recente abstract di una conferenza riporta anche differenze nell'accumulo di residui per liquidi addensati con amido di mais rispetto ad addensanti di gomma di xantano, e attribuisce queste differenze alle proprietà coesive del bolo giudicate soggettivamente. Allo stesso modo, diversi articoli esaminati hanno rivelato che alcuni agenti addensanti producevano prodotti con profili reologici o di proprietà dei materiali diversi, come suggerito in altri studi precedenti, e si è dimostrato che richiedevano diversi gradi di elaborazione orale e si è suggerito che avessero diverse velocità di flusso. Pertanto, è ingenuo e non appropriato supporre che liquidi addensati a viscosità simili utilizzando agenti diversi si comporteranno in modo simile nell'orofaringe. La possibilità che proprietà diverse dalla viscosità possano avere rilevanza clinica è sia intrigante che importante e pone una sfida alla comunità scientifica nello sviluppo di studi rigorosi che caratterizzino tali proprietà secondo metodi convalidati, al fine di esplorare tali fenomeni.

6 Strategie nutrizionali
Premessa
Nell'ambito della gestione nutrizionale dei pazienti affetti da disfagia, è essenziale ricordare la presenza dei disturbi del gusto, poiché tali alterazioni sensoriali possono influenzare significativamente l'aderenza ai protocolli dietetici e la qualità della vita del paziente. Nel paziente disfagico le alterazioni del gusto e la progressiva perdita sensoriale possono portare alla mancanza di interesse progressiva verso il cibo oltre ai possibili fenomeni di malnutrizione.
Facendo una panoramica generale, alcuni possibili strategie alimentari utili a contrastare la perdita del gusto fanno riferimento all’assunzione di cinque pasti al giorno.Naturalmente la suddivisione prevede che i pasti siano organizzati secondo porzioni non abbondanti. Ciò prevede che l’organizzazione dei piatti dovrebbe includere pietanze via via differenti. Il concetto di base è quello di introdurre piccole quantità che via via cambiano.
Mangiare ciò che più soddisfa in un determinato momento può sembrare banale, in realtà assumere i propri cibi preferiti può aiutare la stimolazione dell’appetito. Prediligere il gusto è un fattore importante, in situazioni di alterazione di quest’ ultimo infatti è consigliato l’utilizzo di marinature con agrumi o agrodolci per camuffare alcuni alimenti che tendono ad avere sapori amari o ferrosi come le carni bovine. Alcuni tra gli aromi maggiormente consigliati sono: curry, curcuma, zenzero ed erbe aromatiche dal sapore deciso. Una preferenza tra le alternative disponibili potrebbe essere quella di utilizzare cibi freschi e dissetanti come frutta, verdura e frullati preparati con il latte o yogurt.
6.1 Migliorare il sapore e la consistenza
L'assunzione di cibo ha due scopi: nutrimento e piacere. Il primo è un bisogno fisiologico, il secondo è psicologico. Di solito l'assunzione di cibo è correlata positivamente al grado di fame. Diverse diete esistenti consentono ai pazienti di scegliere tra un'ampia gamma di ingredienti, metodi di preparazione e sapori in base alle proprie preferenze. Tuttavia, i pazienti con disfagia potrebbero aver bisogno più del gusto che dell’appetito, infatti più il cibo ha un sapore migliore più si mangia, anche se questa regola vale un pò per tutti. Pertanto, oltre alla morbidezza, all'uniformità della consistenza, alla ricchezza, alla viscosità e alla facilità di masticazione e deglutizione, anche l'aspetto di un piatto dovrebbe stimolare l'appetito e consentire al paziente di anticiparne il sapore. Alcuni rapporti hanno confrontato il cibo frullato standard con le puree 3D modellate. Dopo la modifica, le puree modellate assomigliavano meglio all'aspetto originale di quel cibo. Il gusto, la consistenza e l'aspetto migliorarono notevolmente, rendendo tali alimenti più appetibili per i pazienti e più comodi per gli infermieri da nutrire. I risultati del rapporto indicavano che l'assunzione di cibo era aumentata del 15%, l'assunzione di energia era aumentata del 41% e l'assunzione di proteine era aumentata del 36%. 16 Uno studio di Germain et al. ha anche scoperto che il peso medio dei pazienti nel gruppo di trattamento era aumentato di 3,9 kg, mentre il gruppo di controllo aveva perso in media 0,8 kg.17 Le ricette in questo studio incorporavano i gusti dei pazienti nella progettazione del colore, dell'aroma, del gusto e della forma del cibo. Inoltre si valutava lapProgettazione di spuntini tra i pasti insieme all’ausilio degli integratori nutrizionali di cui parleremo nel paragrafo successivo, per garantire energia e nutrizione giornaliere sufficienti .
Il tempo tra la colazione e il pranzo dei pazienti è spesso troppo breve (circa 3-4 ore) e il tempo tra la cena e la colazione può essere superiore a 12 ore. Pertanto, spuntini ad alto contenuto energetico tra i pasti con consistenze adeguate sono fondamentali per soddisfare i requisiti nutrizionali. Normalmente, gli spuntini del mattino e del pomeriggio sono costituiti da piccole torte e frutta, mentre lo spuntino serale può consistere in un bicchiere di latte o yogurt e biscotti. Tuttavia, per i pazienti con disfagia, mangiare spuntini piccoli e ricchi di energia tra i pasti può promuovere l'assunzione massima di nutrienti, soprattutto per i pazienti con scarso appetito. Se l'assunzione giornaliera dietetica di un paziente non raggiunge il 60% del fabbisogno target, si dovrebbe ricorrere ai supplementi. La quantità raccomandata di integratori alimentrari dovrebbe essere sufficiente per raggiungere l'assunzione giornaliera raccomandata di energia e proteine, o almeno 400-600 Kcal in più rispetto all'assunzione calorica giornaliera richiesta.
6.2 Integratori nutrizionali (ONS)
Gli integratori nutrizionali orali (ONS) sono liquidi sterili, semisolidi o polveri, che forniscono macro e micro nutrienti. Sono ampiamente utilizzati in contesti sanitari acuti e comunitari per individui che non sono in grado di soddisfare i propri requisiti nutrizionali attraverso la sola dieta orale. L'uso degli ONS (oral nutritional supplements) nel Regno Unito ad esempio, deve essere approvato dall'Advisory Committee on Borderline Substances (ACBS) ed il loro utilizzo come già precedentemente accennato è indicato anche nel supporto delle terapie nutrizionali in caso di disfagia, i pazienti con problemi di deglutizione infatti richiederanno la valutazione di un logopedista prima che gli integratori nutrizionali possano essere prescritti in sicurezza e prima dell'input dietetico. Possono essere prescritti a breve termine durante la malattia acuta, ma anche per individui con condizioni croniche a lungo termine, il loro ruolo dunque è quello di integrare l'assunzione nutrizionale. E’ bene ricordare che gli integratori nutrizionali orali non devono essere utilizzati come trattamento di prima linea, inizialmente si dovrebbe adottare un approccio "cibo prima di tutto”. Naturalmente, se dovesse verificarsi un cambiamento positivo verso il raggiungimento degli obiettivi, questo va incoraggiato e mantenuto, inoltre un'ulteriore revisione deve essere organizzata fino al raggiungimento degli obiettivi. Tutto ciò significa offrire consigli sulla fortificazione degli alimenti per aumentare le calorie e le proteine negli alimenti quotidiani, saranno quindi necessari spuntini aggiuntivi per soddisfare i requisiti di coloro che hanno poco appetito. Alcuni integratori nutrizionali sono disponibili per l'acquisto senza ricetta nei supermercati o nelle farmacie (solitamente in polvere da mescolare con latte o acqua), ma la maggior parte di questi è disponibile solo su prescrizione, idealmente seguendo il consiglio di un dietologo registrato. Gli ONS contengono spesso macronutrienti (proteine e/o energia) e micronutrienti (vitamine e minerali) a vari livelli di concentrazione. Pertanto, non tutti i prodotti che rientrano all’interno di questa categoria risultano nutrizionalmente completi, il che significa che non possono essere utilizzati come unica fonte di nutrimento. La valutazione dietetica individuale terrà conto dei requisiti nutrizionali e delle preferenze di gusto e consistenza per garantire che venga consigliata una prescrizione personalizzata. Gli integratori alimentari devono essere usati con cautela in coloro che soffrono di disfagia per garantire la corretta consistenza, abbiamo già descritto precedentemente i fattori che determinano le difficoltà deglutitorie, i fattori che espongono al rischio soffocamento e la derivante necessità di prestare la massima attenzione sulla consistenza dei cibi somministrati. È infatti possibile aggiungere addensanti per ottenere la consistenza consigliata per i diversi livelli di disfagia e dovrebbe essere offerta una gamma di aromi per evitare altresì l'affaticamento del gusto.
Esiste poi un gruppo emergente di ONS progettati per individui di età superiore ai 65 anni che possono essere a rischio di carenza di vitamina D. Altri prodotti possono essere utili in pazienti con condizioni mediche specifiche in cui l'equilibrio di liquidi ed elettroliti è importante. I pazienti con intestino corto potrebbero non tollerare gli ONS iperosmolari in quanto potrebbero aumentare le perdite di stomia. In ogni caso il loro utilizzo strettamente monitorato dallo specialista, può essere protratto anche per lunghi periodi, fino al miglioramento delle condizioni del paziente.
La valutazione della presenza di deficit nutrizionali è essenziale al fine dell’appropriata somministrazione dei supplementi orali ed un BMI inferiore a 18,5 kg/m2 risulta già un indice di rischio, così come una perdita di peso involontaria superiore al 10% negli ultimi 3-6 mesi. In ogni caso le linee guida suggeriscono che i pazienti per i quali gli integratori sono l'unica fonte di nutrimento, devono essere indirizzati al servizio dietetico senza indugio. Numerosi integratori a base di neurotrofici, acido alfalipoico, vitamine e altri nutrienti possono offrire un supporto significativo. I pazienti che assumono integratori orali devono essere sottoposti a controlli regolari ogni 3 mesi, per valutare i progressi verso gli obiettivi e se vi è una continua necessità di prescrizione. Vanno monitorati i parametri che riguardano peso/BMI , ma se non si riesce a pesare il paziente, registrare altre misure per valutare se il peso è cambiato, ad esempio circonferenza del braccio medio-superiore, vestiti/anelli/orologio più larghi o più stretti, e valutazione visiva cambiamenti nell'assunzione di cibo. Quando gli obiettivi del trattamento sono raggiunti, è preferibile interrompere le prescrizioni di ONS e continuare con l'approccio del cibo, se necessario. Gli integratori non deve essere prescritto a lungo termine e come già detto prima, al raggiungimento degli obiettivi l'assunzione di integratori dovrebbe essere ridotta gradualmente massimizzando l’apporto nutrizionale. Risulterà opportuna la programmazione dei check nutrizionali per verificare che non ci siano recidive del problema.
6.3 Approccio nutrizionale nel paziente disfagico
Dal momento in cui l’assunzione di cibo in termini di volume può risultare ridotta per motivi legati alla mancanza di appetito, una dieta ad alto contenuto energetico contenente ingredienti naturali potrebbe presentare diversi vantaggi. In prima battuta la facile adattabilità per i pazienti anziani che non assumono altri integratori nutrizionali, la facile preparazione dei pasti in qualsiasi cucina di ospedale o casa di cura, e fattori economici dal momento che l’aumento del contenuto energetico del cibo rappresenta una strategia che non incide in modo significativo da questo punto di vista. Alla luce di ciò, pensare di aggiungere grassi come mezzo di fortificazione nutrizionale può anche migliorare il gusto e la palatabilità degli alimenti. Sebbene il rapporto grassi/energia di una dieta non debba generalmente superare il 50%, i pazienti che richiedono più energia possono trarre beneficio da questa dieta nel breve termine. I grassi come quelli contenuti nell'olio di cocco, classificati a catena media, quelli dell'olio di semi di lino, e quelli dell’olio d'oliva ricco di acidi grassi monoinsaturi, possono aumentare la densità energetica.
Sulla base pratica, il piano alimentare andrebbe indirizzato sull’idea di un’alimentazione varia che si riflette nelle ricette fornite. Si possono utilizzare alimenti come la carne, una verdura, uno spuntino e un frutto come unità di base, mentre per quanto riguarda il volume e la densità dei nutrienti di ogni unità, essi vengono modificati appositamente nella loro consistenza per soddisfare le diverse esigenze dei pazienti con disfagia. Il latte dovrebbe essere utilizzato al posto dell’acqua durante la preparazione dei cibi, ed i carboidrati sottoforma di destrine, andrebbero poi aggiunti in modo che ogni porzione fornisca 250 Kcal di energia. Per ciò che concerne la scelta che prevede l’utilizzo del latte, va considerato che gli alimenti con consistenza modificata vengono solitamente ammorbiditi dalla cottura con una quantità di acqua relativamente grande e quindi forniscono un contenuto nutrizionale inferiore rispetto alle diete convenzionali. Un altro aspetto importante è che i pazienti potrebbero aver bisogno di consumare un volume di cibo che supera la tolleranza del loro tratto gastrointestinale per raggiungere lo stesso livello di nutrienti di una dieta normale. Per questo, gli ingredienti per una porzione di ogni tipo di alimento dalla consistenza modificata vengono determinati in base alle abitudini alimentari del paziente e al volume di ogni pasto. Il peso di ogni porzione è simile a quello del cibo convenzionale ed il contenuto nutrizionale di una porzione standard viene calcolato in ogni tipo di alimento. E’ utile ricordare che uno sbilanciamento della quota calorica unita alla cattiva gestione dei pasti rappresenta un potenziale aspetto che contribuisce in modo cruciale a possibili quadri di denutrizione nei pazienti con disfagia, per questo quando si progettano le ricette, bisogna considerare la quantità di cibo e il grado di sazietà di ogni pasto. In un pasto standard la quota proteica introdotta va in misura di 14g per fornire una quota calorica di circa 150 Kcal di energia. Per ciò che riguarda verdura e frutta, questi forniscono rispettivamente 70 Kcal e 90 Kcal di energia.
Per le ricette a base di cereali si può prevedere l’utilizzo del riso con una grammatura di 25g, ed un rapporto di 1:2 tra riso e acqua. Si aggiunge poi la quantità appropriata di modificatore di consistenza alimentare e si frulla con un robot da cucina. Per ciò che riguarda la carne invece, secondo le raccomandazioni dell'Expert Consensus, ogni porzione di carne dovrebbe pesare 50 g e il cibo rappresentativo è maiale magro. Il metodo di preparazione prevede di aggiungere acqua o zuppa al piatto cucinato con un rapporto cibo/acqua (o zuppa) di 1:1. Si aggiunge sempre la quantità appropriata di modificatore di consistenza del cibo e frullare con un robot da cucina. Lo spessore del cibo frullato è solitamente determinato dal peso dell’addensante commerciale. Nelle ricette di verdure, una porzione dovrebbe pesare 125 g, con possibilità di includere gli spinaci e le altre verdure a foglia indistintamente. Si utilizzano i piatti tradizionali di verdure come modello, per poi modificarne la consistenza attraverso l’uso dell’addensante. Poiché il contenuto di umidità varia per ogni verdura, il rapporto tra cibo e acqua (o succo di verdura) dovrebbe essere regolato in base al contenuto di umidità della verdura (generalmente da 1 a 0,6-0,8). Per questo motivo andrebbe aggiunta la quantità appropriata di addensante per poi frullare il tutto con un robot da cucina.
Infine la frutta: secondo le raccomandazioni dell'Expert Consensus, una porzione di frutta dovrebbe pesare 200 g, con le arance come frutto rappresentativo. Poiché la frutta ha un alto contenuto di acqua, non è richiesta acqua aggiuntiva quando si preparano le puree di frutta, ma si aggiunge la quantità appropriata di addensante.
Una combinazione alimentare potrebbe prevedere: 160 ml di latte, 60 g di uova o 25 g di fagioli misti, aggiungendo la quantità appropriata di modificatore di consistenza alimentare e frullando con un robot da cucina.
6.4 Diete specifiche per livelli di disfagia
La disfagia si manifesta attraverso quattro distinti livelli che ne caratterizzano la gravità, classificati sulla base della tipologia del disturbo ed alla fase di deglutizione in cui questo si verifica. Risulta dunque opportuno indicare una dieta specifica, che possa adattarsi alle caratteristiche del quadro clinico generale ed opportunamente composta da alimenti e bevande con caratteristiche adeguate ai problemi specifici di masticazione e deglutizione del paziente.
Dieta per disfagia di grado 1
Individui appartenenti al livello 1 evidenziano una funzione masticatoria assente e una capacità deglutitoria profondamente compromessa; ne consegue una completa impossibilità nel far transitare alimenti, sia solidi che fluidi, verso lo stomaco. La dieta raccomandata per questi soggetti prevede cibi di natura semiliquida ed uniforme, la cui densità può oscillare, conformemente alla tolleranza di ciascuno, da quella paragonabile a un succo di frutta fino a quella di una vellutata o di una preparazione cremosa. È fattibile rendere più fluidi gli alimenti tramite l'impiego di liquidi oppure di condimenti che non ne alterino il profilo organolettico, come ad esempio bevande a base lattea, sia calde che fredde, o brodi di carne privi di particelle solide. L'utilizzo di sostanze grasse quali olio, burro, margarina, così come di panna e salse del tipo besciamella, è ammesso. Risultano invece categoricamente proibiti quegli alimenti che tendono a sbriciolarsi o che sviluppano una consistenza collosa. I liquidi puri non sono permessi; è imperativo che vengano preventivamente trattati con idonei prodotti modificatori della consistenza, disponibili presso le farmacie, per alterarne la fluidità.
Dieta per disfagia di grado 2
Chi ha una capacità di masticazione ridotta dovrebbe attenersi alle indicazioni inerenti alla una dieta di secondo livello, inoltre in questo caso la funzione deglutitoria risulta fortemente compromessa. Per fa sì che l’alimentazione rispetti gli standard prefissati per il livello 2, i cibi devono avere la consistenza di una purea o del budino cremoso. Sono indicati i cibi dai sapori forti speziati o in agrodolce per stimolare la salivazione e favorire così il riflesso di deglutizione. Rientrano nella categoria dei cibi vietati gli alimenti in pezzi interi o con doppie consistenze come ad esempio le minestre o le zuppe con crostini, gli alimenti non compatti come il riso, i legumi, pane e crackers. L’assunzione di acqua o altri liquidi è fortemente rischiosa. Per ciò che riguarda gli alimenti e le bevande, questi possono essere modificati con gli addensanti attualmnete disponibili.
Dieta per disfagia di grado 3
Qui la masticazione risulta compromessa. Il cibo deve essere morbido senza parti filamentose, sempre cotto o tritato ma non serve frullare. Gli alimenti non devono essere croccanti o secchi. Consultare il medico per assumere liquidi.
Dieta per disfagia di grado 4
Una dieta di quarto livello è certamente adatta a chi è in grado di assumere alimenti facilmente masticabili e di deglutire solidi e liquidi. In questo caso, come abbiamo detto in precedenza, il paziente ha un buon controllo della deglutizione dal momento che risulta capace di gestire liquidi che possono essere anche leggermente o per nulla densi come l’acqua. In ogni caso, anche qui può risultare preferenziale una lista di cibi che consentono di gestire l’assunzione di alimenti entro dei margini di sicurezza ragionevoli.
7 Nutrizione enterale
Il ruolo della nutrizione nell'assistenza ai pazienti è diventato parte della medicina tradizionale verso la fine degli anni ’60, da quel momento, una serie di studi che hanno confrontato la nutrizione parenterale con quella enterale hanno suggerito che la via enterale di alimentazione causa meno complicazioni rispetto alla via parenterale. Un'attenta revisione dei dati mostra che il supporto nutrizionale può aumentare il rischio di complicazioni quando somministrato a pazienti ben nutriti, obesi o che ad esempio soffrono di iperglicemia. Per tale ragione evitare la sovralimentazione e l'iperglicemia è di fondamentale importanza. In questo contesto, la nutrizione enterale, per la quale la tolleranza gastrointestinale limita la sovralimentazione, può proteggere il paziente.
La nutrizione enterale fornisce macro e micronutrienti essenziali a individui che non riescono a mantenere un apporto orale sufficiente a soddisfare le proprie esigenze nutrizionali, all’atto pratico consiste nell’infusione continua, intermittente oppure in bolo, di miscele nutritive direttamente nel tratto digestivo del paziente. Risulta più comunemente richiesta per condizioni neurologiche che compromettono la funzione di deglutizione, come ictus, sclerosi laterale amiotrofica e morbo di Parkinson, ed in ogni caso ha lo scopo di reintegrare lo stato nutrizionale del paziente qualora non fosse fisiologicamente possibile. Anche l'incapacità di deglutire dovuta alla disfagia può richiedere l'uso di nutrizione enterale. Questa può essere a breve o lungo termine e somministrata per via gastrica o post-pilorica. La durata prevista e il sito di alimentazione determinano il tipo di sondino utilizzato. Sono disponibili molte formule alimentari commerciali per questo tipo di intervento ed oltre alle formulazioni standard, sono disponibili anche formule specifiche per la malattia, basate su peptidi. Diversi altri fattori devono essere presi in considerazione quando il paziente viene alimentato attraverso questo sistema, tra cui tempi e velocità di inizio, regime di avanzamento, modalità di alimentazione e rischio di complicazioni. Una valutazione attenta e completa del paziente aiuterà a garantire che la nutrizione sia nutrizionalmente completa, clinicamente appropriata e venga somministrata in modo sicuro. La nutrizione enterale è necessaria negli individui che non sono in grado di mantenere un adeguato apporto nutrizionale per via orale ed è preferibile alla nutrizione parenterale, che è associata a una maggiore incidenza di effetti collaterali come iperglicemia, anomalie elettrolitiche e tassi di infezione, nonché complicazioni a lungo termine come malattie epatiche e malattie metaboliche delle ossa. Questa tipologia di nutrizione è più fisiologicamente naturale e aiuta a mantenere l'integrità intestinale che supporta la funzione immunitaria e protegge dall'atrofia intestinale.
Un apporto inadeguato dal punto di vista nutrizionale può essere causato da una varietà di ragioni fisiologiche o mediche, la più comune è la disfagia, precipitata da condizioni neurologiche croniche come il morbo di Parkinson o la sclerosi laterale amiotrofica, così come da disfunzione temporanea o permanente del meccanismo di deglutizione a seguito di incidenti cerebrovascolari o condizioni come tumori della testa e del collo. Sono da considerare inoltre i livelli ridotti di coscienza o gli stati mentali significativamente alterati a causa di demenza, ventilazione meccanica ed encefalopatia epatica o metabolica.
Solitamente la nutrizione enterale non è raccomandata in caso di tratto gastrointestinale non funzionale. Condizioni come fistole, ostruzioni intestinali, ileo paralitico o prolungato e ischemia mesenterica precludono la capacità di fornire tale supporto e richiedono nutrizione parenterale. Nei casi in cui un individuo non può assumere nutrizione per via orale e il tratto gastrointestinale non è accessibile, potrebbe essere necessaria anche la nutrizione parenterale. Nelle prime fasi di malattia critica, la ricerca ha dimostrato che non vi è alcuna differenza nei risultati clinici in pazienti che vengono nutriti con nutrizione enterale rispetto alla nutrizione parenterale per brevi periodi di tempo (da 5 a 7 giorni). Va detto che il supporto enterale potrebbe essere controindicato nelle persone che sono alla fine della vita e non desiderano ricevere interventi medici e nutrizionali aggressivi, inoltre nei soggetti con demenza avanzata, la ricerca ha dimostrato che la fornitura di nutrizione enterale non migliora la qualità della vita.
Esistono fattori clinici estremamente importanti che necessitano di essere presi in considerazione per i pazienti gravemente malati che necessitano di nutrizione enterale, come ad esempio l'instabilità emodinamica. Questa condizione è solitamente un'indicazione per ritardare l'inizio della tipologia di supporto nutrizionale. Inoltre l'alimentazione enterale mentre un paziente è ipotensivo può causare ischemia intestinale poiché il corpo dà priorità al flusso sanguigno verso organi più vitali, come cuore, cervello e polmoni, lasciando il tratto gastrointestinale con una perfusione sanguigna insufficiente. Sebbene questa sia una complicazione rara, gli effetti possono essere devastanti, tra cui intestino necrotico che richiede resezione e aumento della mortalità.
Alcuni studi infine hanno dimostrato che i pazienti con tumore alla testa/collo in cui i sondini di alimentazione sono stati posizionati prima dell'inizio dei trattamenti contro il cancro hanno avuto risultati complessivamente migliori, tra cui la prevenzione della perdita di peso, una riduzione dei ricoveri ospedalieri e una migliore qualità della vita, rispetto a coloro che non lo hanno fatto. La NE precoce nei pazienti con pancreatite acuta grave è associata a una mortalità inferiore, a una minore incidenza di insufficienza multiorgano e a una ridotta necessità di interventi chirurgici.
7.1 SOLUZIONI STANDARD PER LA NUTRIZIONE ENTERALE
I pazienti ad alto rischio di rialimentazione sono quelli con malnutrizione o scarso apporto nutrizionale per un periodo prolungato. Nella rialimentazione, il destrosio viene rapidamente acquisito dalle cellule, con conseguenti spostamenti di elettroliti extracellulari a intracellulari. Anche la tiamina può esaurirsi in quanto è un cofattore necessario per i processi metabolici correlati al glucosio. Il segno distintivo della rialimentazione è l'ipofosfatemia, sebbene siano comuni anche ipokaliemia e ipomagnesemia. Gli elettroliti carenti devono essere sostituiti prima di iniziare la nutrizione enterale e controllati / sostituiti quotidianamente secondo necessità fino a stabilizzazione. Deve essere somministrata anche una tiamina supplementare. Nell'alimentazione basata sul volume, viene determinato un volume obiettivo giornaliero totale di formula EN (Enteral Nutrition) e viene calcolata una velocità di raggiungimento dell’obiettivo in base al numero di ore in cui è programmata l’infusione. Questa tipologia di nutrizione può essere classificata come standard, oppure basata su peptidi, immunomodulanti, con caratteristiche specifiche per malattia e frullate. La composizione di queste formule varia a seconda del produttore, ma condivide caratteristiche simili. I medici devono essere consapevoli dell’efficacia a favore dell'uso di formule speciali per malattie o condizioni cliniche specifiche.
Le formule standard in ogni caso contengono nutrienti intatti, solitamente con carboidrati sotto forma di maltodestrine e sciroppo di mais, proteine di soia o caseinati e grassi come olio di cartamo, canola o soia. Sono disponibili in diverse concentrazioni, ovvero da 1 a 2 kcal/mL; formule più concentrate possono essere appropriate per individui con condizioni che richiedono restrizioni di liquidi, come insufficienza cardiaca e malattie renali. Alcune formule standard hanno fibre, solitamente una combinazione di fibre solubili e insolubili, mentre altre sono prive di fibre.
Le linee guida per il supporto nutrizionale nelle malattie critiche affermano che una formula standard con o senza fibre può essere tollerata dalla maggior parte dei pazienti in terapia intensiva. Le formule contenenti fibre dovrebbero essere evitate nei pazienti emodinamicamente instabili e a rischio di ischemia intestinale. Inoltre, le formule contenenti fibre non dovrebbero essere utilizzate di routine per promuovere la regolarità intestinale o prevenire la diarrea in questa popolazione di pazienti. Sebbene le formule standard possano essere utilizzate per la maggior parte dei pazienti gravemente malati, la malattia critica comporta un fabbisogno proteico elevato e le formule standard generalmente non sono sufficientemente ricche di proteine per soddisfare tali fabbisogni senza l'uso di un modulare proteico supplementare. Si evidenzia il fatto che le formule epatiche sono molto povere di proteine (fino al 10% delle calorie totali) con un profilo aminoacidico modificato, vale a dire un rapporto aumentato tra aminoacidi a catena ramificata e aromatici. Tuttavia, non vi è alcun beneficio noto per queste formule, pertanto il loro uso non è raccomandato. In ogni caso la restrizione proteica può causare o peggiorare la malnutrizione e pertanto non è raccomandata per i pazienti con malattia epatica allo stadio terminale. Inoltre, la restrizione proteica non è più raccomandata nei pazienti con encefalopatia epatica poiché aumenta il catabolismo proteico ed ha dimostrato di peggiorare i risultati clinici.
Le formule a base di peptidi, possono essere utilizzate in pazienti con malassorbimento o che hanno dimostrato intolleranza alle formule standard. Queste formule sono più facili da digerire poiché le proteine vengono idrolizzate in peptidi a catena piccola e le fonti di grassi includono trigliceridi a catena media e/o lipidi strutturati da olio di pesce. Le formule a base di peptidi sono generalmente ricche di proteine; alcune possono contenere fino al 25-35% delle calorie totali dalle proteine e sono quindi utili nei pazienti gravemente malati, specialmente in quelli che ricevono calorie aggiuntive da soluzioni che richiedono un apporto inferiore per evitare un'alimentazione eccessiva. Molte formule a base di peptidi contengono anche quantità maggiori di micronutrienti antiossidanti, come le vitamine C, D, E e selenio; e gli acidi grassi omega-3 acido eicosapentaentoico (EPA) e acido docosaesaenoico (DHA).
Alcune formule a base di peptidi sono considerate immunostimolanti o immunomodulanti. Oltre ai componenti antiossidanti aggiunti presenti in altre formule a base di peptidi, contengono arginina e glutammina. La ricerca sull'uso di formule immunomodulanti ha dimostrato risultati migliori, come tassi di infezione ridotti, durata ridotta della degenza ospedaliera e durata ridotta della ventilazione meccanica nei pazienti traumatizzati e chirurgici in terapia intensiva. Le linee guida di supporto nutrizionale in terapia intensiva raccomandano di prendere in considerazione le formule immunomodulanti solo nei pazienti post-operatori in terapia intensiva e con lesioni cerebrali traumatiche. Si ipotizza che l'arginina supplementare possa causare effetti collaterali negativi nei pazienti settici a causa del ruolo dell'arginina nella produzione di ossido nitrico, che può peggiorare la stabilità emodinamica. Per questo motivo le linee guida in questi casi non raccomandano l'uso di formule contenenti arginina.
In caso di iperglicemia, le formule sviluppate a favore dei pazienti sono più povere di carboidrati, più ricche di grassi (solitamente sotto forma di acidi grassi monoinsaturi) e contengono fibre. Alcuni studi hanno dimostrato che queste formule possono migliorare il controllo della glicemia, mentre altri no. In una recente revisione, alcuni autori hanno concluso che non vi erano prove sufficienti per promuovere l'uso di formule a basso contenuto di carboidrati. Anche l'uso a lungo termine di queste formule non è stato sufficientemente studiato; pertanto, i potenziali effetti collaterali o complicazioni a lungo termine sono al momento sconosciuti.
In ogni caso l’utilizzo di formule a basso tenore di carboidrati non è esente da controindicazioni che devono essere opportunamente considerate prima della loro relativa somministrazione. Queste formule infatti dovrebbero essere evitate nei pazienti con svuotamento gastrico ritardato, malassorbimento dei grassi o altre condizioni in cui un'elevata assunzione di grassi non è raccomandata. Dovrebbero inoltre essere evitate in alcuni pazienti gravemente malati, vale a dire quelli a rischio di ischemia o ostruzione intestinale in cui l'assunzione di fibre è controindicata.
7.2 TIPOLOGIE DI FORMULE PER LA NUTRIZIONE ENTERALE
Il panorama della nutrizione enterale si articola in diverse formulazioni liquide, disponibili in commercio e classificate principalmente in base al grado di complessità dei loro macronutrienti. Questa distinzione permette di scegliere la soluzione più adatta alle capacità digestive e alle esigenze metaboliche del singolo paziente. La categoria più diffusa è rappresentata dalle formule polimeriche. Queste forniscono una dieta nutrizionalmente completa e bilanciata, contenendo macronutrienti (proteine, carboidrati, grassi) nella loro forma integra. Generalmente prive di lattosio e talvolta arricchite con fibre, sono pensate per pazienti con una funzione digestiva sostanzialmente normale. Esistono anche versioni basate su alimenti frullati. Per i pazienti con capacità digestive o assorbitive compromesse, si ricorre invece a miscele parzialmente o completamente idrolizzate (note anche come elementari). In queste formulazioni, le proteine sono già scomposte in peptidi o aminoacidi liberi, rendendole più facili da assimilare. Solitamente presentano un basso contenuto di grassi, privilegiando i trigliceridi a catena media (MCT). Questa categoria si estende fino a includere le formule specialistiche, progettate per quadri clinici specifici come l'insufficienza renale, il diabete o la necessità di supportare la risposta immunitaria. Mentre alcune di queste soluzioni rispondono a esigenze cliniche consolidate, per altre l'evidenza di un reale beneficio clinico che ne giustifichi il costo è ancora in discussione. Infine, per una personalizzazione ancora più spinta del regime nutrizionale, esistono i prodotti modulari. A differenza delle formule complete, questi moduli forniscono un singolo nutriente (come proteine in polvere) o una combinazione limitata (es. carboidrati e grassi). Il loro scopo è integrare una formula di base o il cibo comune per raggiungere target specifici, ad esempio per aumentare l'apporto proteico in pazienti con fabbisogni elevati o per gestire problematiche come stipsi o diarrea tramite l'aggiunta di fibre.
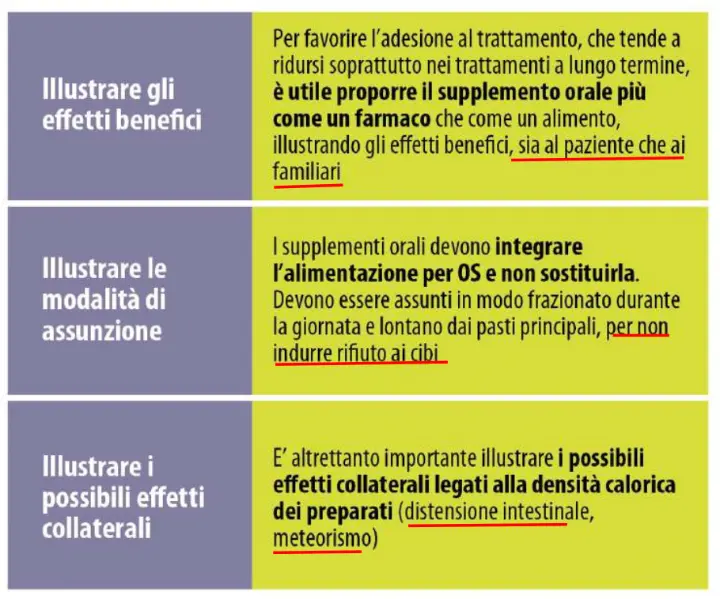
Disclaimer: questo articolo tratta argomenti di carattere medico che ho avuto il piacere di approfondire attraverso la stesura della mia Tesi di Laurea. A tal proposito si precisa che lo scopo di quanto riportato è puramente informativo, non sostituisce in alcun modo il parere dello specialista e vuole essere una semplice condivisione del mio lavoro con i lettori del blog.
Pertanto declino categoricamente ogni tipo di responsabilità derivante dall'utilizzo delle informazioni riportate all'interno dell' articolo.
Ricorda: ogni tuo dubbio necessita del supporto medico adeguato, non affidarti MAI al web.
Bibliografia
Nutritional Academy. La prevalenza della disfagia orofaringea. [Online]. Nutritional Academy, 2024. Disponibile da: https://www.nutritionalacademy.it/aree-terapeutiche/disfagia/la-prevalenza-della-disfagia-orofaringea
Ludlow, C.L. Central Nervous System Control of Swallowing. Gastroenterology Clinics of North America, 2015, vol. 44, no. 4, p. 515-535.
Ferrand, P. Neurology of Swallowing and Dysphagia. American Journal of Speech-Language Pathology, 2013.
Springer Healthcare Italia. Disfagia in oncologia: fattori predisponenti, aggravanti e prognostici. [Online]. Springer Healthcare Italia, 2024. Disponibile da: https://springerhealthcare.it/mr/archivio/disfagia-in-oncologia-fattori-predisponenti-aggravanti-e-prognostici/
Karisik, Anel, et al. Comorbidities associated with dysphagia after acute ischemic stroke. BMC Neurology, 2024. Disponibile da: https://pubmed.ncbi.nlm.nih.gov/39342159/
King, Suzanne N., et al. Pathophysiology of Radiation-Induced-Dysphagia in Head and Neck Cancer. 2016 Apr. Disponibile da: https://pmc.ncbi.nlm.nih.gov/articles/PMC5340192/
Steele, Catriona M., et al. The influence of food texture and Liquid Consistency Modification on Swallowing Physiology and Function. 2014 Oct. Disponibile da: https://pmc.ncbi.nlm.nih.gov/articles/PMC4342510/
International Dysphagia Diet Standardisation Initiative. Documento Quadro IDDSI Descrizione Dettagliata 2.0. Tradotto da Luciana Andrini. 2019, pp. 1-2. [PDF]
Steele, Catriona M., et al. The influence of food texture and Liquid Consistency Modification on Swallowing Physiology and Function. European Archives of Oto-Rhino-Laryngology, 2014, vol. 271, no. 10, p. 2731-2740. DOI: 10.1007/s00455-014-9578-x
Chen, Yanqiu, et al. Nutritional Diet Plan for Patients with dysphagia. Asia Pacific Journal of Clinical Nutrition, 2021, vol. 30, no. 2, p. 284-293. DOI: 10.6133/apjcn.202106_30(2).0008.
Guidelines For The Appropriate Use of Oral Nutritional Supplements (ONS) For Adults In Primary Care. 2022. Disponibile da: https://www.northernlincolnshireapc.nhs.uk/wp-content/uploads/2022/05/
Doley, Jennifer. Enteral Nutrition Overview. 2022. Disponibile da: https://pmc.ncbi.nlm.nih.gov/articles/PMC9183034/
Mogensen, Kris M., et al. Formule per la Nutrizione Enterale. Manuale MSD, Set 2024. Disponibile da: https://www.msdmanuals.com/it/professionale/disturbi-nutrizionali/supporto-nutrizionale/nutrizione-enterale
Bapen. Oral Nutrition Supplements(ONS). [Online]. Bapen, 2025. Disponibile da: https://www.bapen.org.uk/education/nutrition-support/nutrition-by-mouth/oral-nutritional-supplements-ons/
Redazione Mypersonaltrainer, Disfagia: Cos'è? Cause, Sintomi e Classificazione, in Mypersonaltrainer.it, Gruppo Mondadori, ultimo aggiornamento 8 febbraio 2024.
Disponibile all'indirizzo: https://www.my-personaltrainer.it/Sintomi/Disfagia